Гальваническая коррозия алюминия – aluminium-guide.com
Следует подчеркнуть, что стойкость алюминия и алюминиевых сплавов к нормальным условиях окружающей среды является очень высокой. Главным источником защиты от коррозии является прочная, самовосстанавливающаяся оксидная пленка, которая всегда присутствует на алюминии в условиях окружающей воздушной атмосферы (рисунок 1).
Рисунок 1 – Естественная защита алюминия от коррозии – поверхностная оксидная пленка [4]
Основные типы коррозии алюминия
Для коррозии алюминия характерны следующие основные типы [4]:
- Общая коррозия
- Щелевая коррозия
- Фреттиниг-коррозия
- Коррозия под напряжением
- Гальваническая коррозия
- Точечная (питтинговая) коррозия
- Межзеренная коррозия
- Подповерхностная коррозия
Рисунок 2 – Общая коррозия алюминия: растворение естественной оксидной пленки
растворами сильных щелочей и некоторых кислот [4]
Рисунок 3 – Щелевая коррозия алюминия [4]
в условиях шероховатого контакта [4]
Рисунок 5 – Коррозия алюминиевых сплавов под напряжением: при некоторых условиях
в сплавах Al-Cu, Al-Mg, Al-Zn-Mg [4]
Рисунок 6 – Гальваническая коррозия алюминиевого сплава
происходит в условиях его мокрого или влажного контакта
с другим, более “благородным” металлом, таким как медь [4]
Рисунок 7 – Питтинговая (точечная) коррозия алюминия
под воздействием хлоридных ионов [4]
Рисунок 8 – Межзеренная коррозия и подповерхностная коррозия [4]
В зависимости от условий окружающей среды, нагружения и функционального назначения детали любой из видов коррозии может явиться причиной преждевременного разрушения.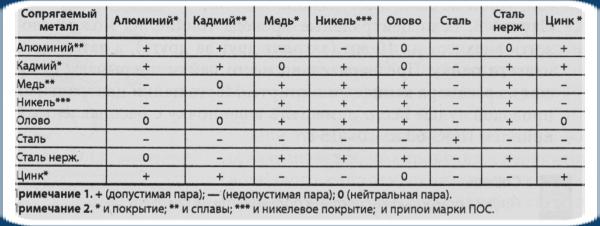
Гальваническая коррозия алюминия
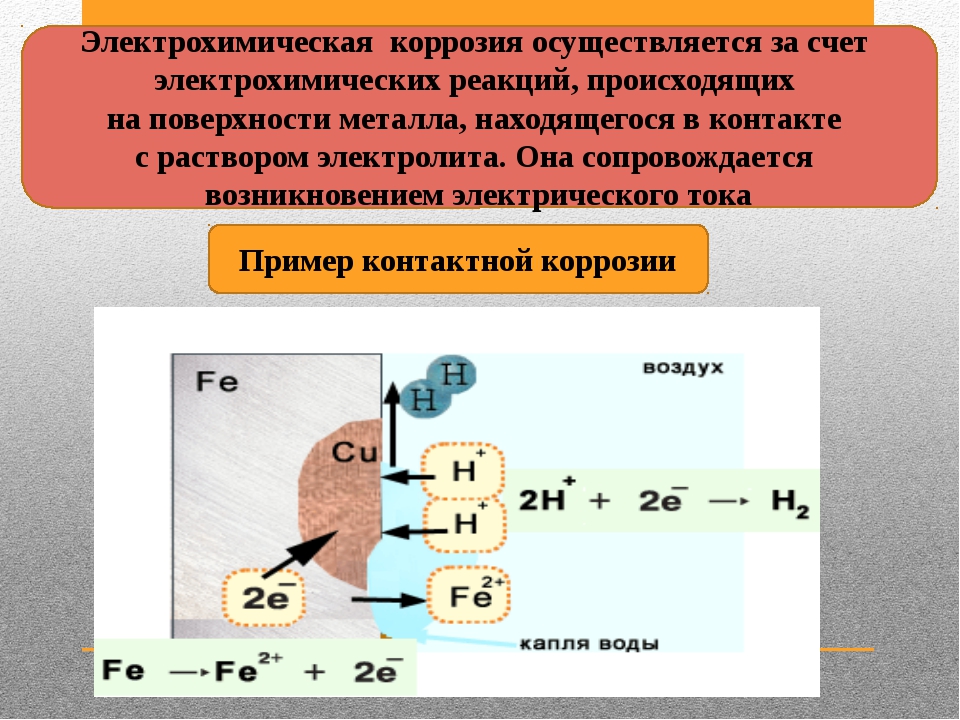
Наиболее частые ошибки проектирования алюминиевых конструкций связаны с гальванической коррозией. Гальваническая или электрохимическая коррозия происходит, когда два разнородных металла образуют электрическую цепь, замыкаемую жидким или пленочным электролитом или коррозионной средой. В этих условиях разность потенциалов между разнородными металлами создает электрический ток, проходящий через электролит, который (ток) и приводит к коррозии в первую очередь анода или менее благородного металла из этой пары.
Сущность гальванической коррозии
Когда два различных металла находятся в прямом контакте с электропроводящей жидкостью, то опыт показывает, что один из них может корродировать, то есть подвергаться коррозии. Это называют гальванической коррозией.
Другой металл не будет корродировать, наоборот, он будет защищен от этого вида коррозии.
Этот вид коррозии отличается от тех видов коррозии, которые могли бы возникнуть, если бы оба эти металлы были помещены раздельно в ту же самую жидкость. Гальваническая коррозия может случиться с любым металлом, как только два различных металла будут находиться в контакте в электропроводящей жидкости.
Внешний вид гальванической коррозии
Внешний вид гальванической коррозии является очень характерным. Эта коррозия не раскидывается по всей поверхности изделия, как это бывает с точечной – питтинговой – коррозий. Гальваническая коррозия плотно локализована в зоне контакта алюминия с другим металлом. Коррозионное воздействие на алюминий имеет равномерный характер, он развивается в глубь в виде кратеров, которые имеют более или менее округлую форму [3[.
Все алюминиевые сплавы подвергаются идентичной гальванической коррозии [3].
Принцип батареи
Гальваническая коррозия работает как батарея, которая состоит из двух электродов:
- катода, где происходит реакция восстановления
- анода, где происходит реакция окисления.

Эти два электрода погружены в проводящую жидкость, которая называется электролитом. Электролит – это обычно разбавленный кислотный раствор, например, серной кислоты, или соляной раствор, например, сульфат меди. Эти два электрода соединены снаружи электрической цепью, которая обеспечивает циркуляцию электронов. Внутри жидкости передача электрического тока происходит путем перемещения ионов. Жидкость, таким образом, обеспечивает ионное электрическое соединение (рисунок 9).
Рисунок 9 – Принцип гальванической ячейки [3]
Рисунок 1 показывает ячейку, в которой электролитом является раствор серной кислоты. Серная кислота полностью диссоциирована в воде (поскольку является сильной кислотой) путем образования ионов Н+, которые определяют кислотность среды. Происходит следующая электрохимическая реакция [3]:
- цинковый анод окисляется:
Zn → Zn2+ + 2e−
на медном катоде восстанавливаются протоны Н+:
2Н+ + 2e− → Н2
Полная реакция имеет вид:
Zn + H2O → Zn(OH)2 + H2
Эта ячейка производит электричество за счет потребления цинка, который выделяется в виде гидроксида цинка Zn(OH)![]()
Для работы ячейки необходимо одновременное выполнение трех условий:
- два различных металла, которые образуют два электрода;
- присутствие электролита;
- непрерывность всей электрической цепочки.
Если хотя бы одно из этих условий не выполняется, например, если нарушается электрический контакт, то ячейка не будет производить электричество, и окисления на аноде не будет происходить (также как и восстановления на катоде).
Условия для гальванической коррозии
Гальваническая коррозия основана на том же самом принципе и для того, чтобы она происходила необходимо одновременное выполнение следующих трех условий [3]:
- различные типы металлов;
- присутствие электролита;
- электрический контакт между двумя металлами.
Различные типы металлов
Для любых металлов, которые относятся к различным их типам, гальваническая коррозия является возможной. Металл с электроотрицательным потенциалом (или более электроотрицательный металл, если они оба электроотрицательные) действует как анод.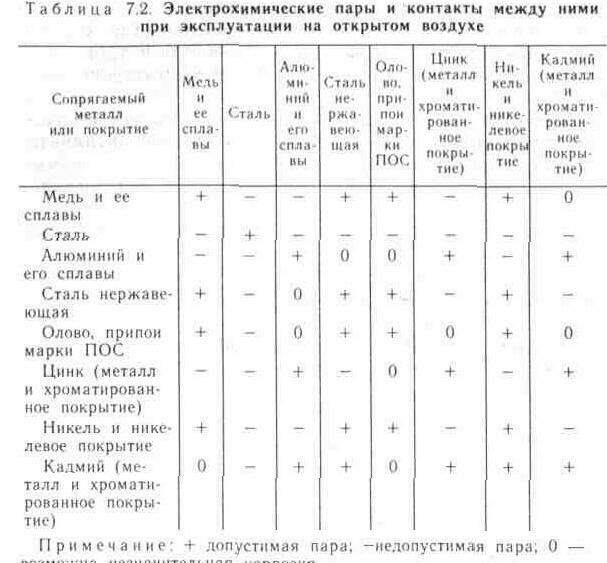
Тенденцию различных металлов образовывать гальванические пары и направленность электрохимического действия в различных коррозионных средах (морской воде, тропическом климате, промышленной атмосфере и т.д.) показывают в так называемых гальванических рядах. Чем далее удалены друг от друга металлы в этих рядах, тем более серьезной может быть электрохимическая коррозия. В разных коррозионных средах эти последовательности металлов могут быть разными (рисунок 10).
Присутствие электролита
Область контакта должна быть смочена водным раствором, чтобы обеспечивать ионную электропроводимость. В противном случае отсутствует возможность для гальванической коррозии.
Электрический контакт между металлами
Электрический контакт между металлами может происходить или путем прямого контакта между двумя металлами, или через крепежное соединение, например, болт.
Рисунок 10 [1]
Как видно из графиков рисунка 10 алюминий и его сплавы становятся анодами в гальванических ячейках с большинством металлов, и алюминий корродирует, как говорят, жертвенно и защищает от коррозии другой металл гальванической пары.
Только магний и цинк, включая и оцинкованную сталь, являются более анодными и поэтому, сами подвергаясь коррозии, защищают от нее алюминий.
Алюминий и кадмий вообще имеют почти одинаковые электродные потенциалы и поэтому ни алюминий, ни кадмий не подвергаются гальванической коррозии. К сожалению, кадмий признан весьма токсичным и все реже применяется, а во многих странах просто запрещен, как антикоррозионная защита.
Гальванические пары
Относительное расположение двух металлов или сплавов в гальваническом ряду указывает только возможность гальванической коррозии, если различие их гальванических потенциалов является достаточно большим. Больше этот ряд ничего не говорит, и особенно ничего – о скорости или интенсивности гальванической коррозии. Она может быть нулевой или несущественной или даже незаметной. Ее интенсивность зависит от типов металлов, которые входят в контакт – гальванической пары.
Пара: алюминий – нелегированная сталь
В строительных конструкциях алюминиевые детали, которые открыты для воздействия климатических и погодных воздействий, могут соединяться винтами из обычной стали.
Это явление имеет следующее объяснение:
- на поверхностях контакта образуются пленки с продуктами коррозии – ржавчины на стали и оксида алюминия на алюминии, которые и замедляют электрохимические реакции.
Пара: алюминий – оцинкованная сталь
Судя по гальваническому ряду, цинк является более электроотрицательным, чем алюминий. Крепеж из оцинкованной стали может, поэтому, применяться для соединения и сборки конструкций из алюминиевых сплавов. Надо помнить, что когда цинковое покрытие станет слишком изношенным, чтобы защищать сталь и алюминий, наступает предыдущий сценарий контакта между алюминием и голой сталью [3] .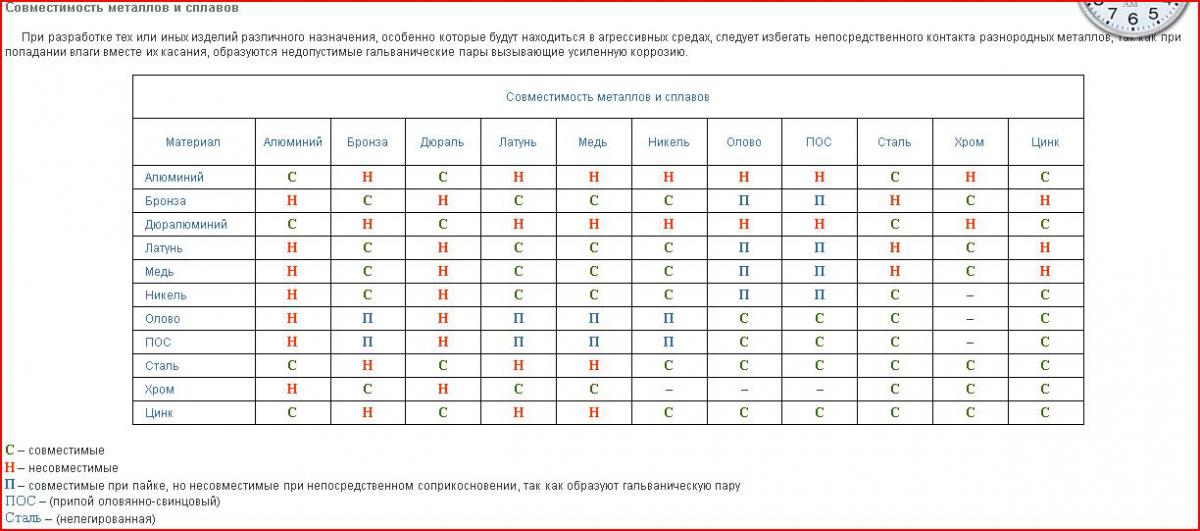
Пара: алюминий – нержавеющая сталь
Хотя и существует большая разность потенциалов между нержавеющей сталью и алюминиевыми сплавами – около 650 мВ, очень редко можно увидеть гальваническую коррозию на алюминии в контакте с нержавеющей сталью. Поэтому алюминиевые конструкции очень часто собираются с применением болтов и винтов из нержавеющей стали [3].
Пара: алюминий – медь
Контакт между алюминиевыми сплавами и медью, а также медными сплавами (бронза, латунь) приводит к совершенно незначительной гальванической коррозии алюминия под воздействием атмосферных условий. Тем не менее, рекомендуется обеспечивать электрическую изоляцию между этими двумя металлами, чтобы локализовать коррозию алюминия.
Необходимо отметить, что продуктом коррозии меди является, так называемая, патина. Эта патина – голубовато-зеленый налет на меди, который состоит в основном из карбоната меди. Эта патина химически воздействует на алюминий и может восстанавливаться с образованием малых частиц меди. Эти медные частицы, в свою очередь, могут вызывать локальную питтинговую коррозию алюминия [3].
Эти медные частицы, в свою очередь, могут вызывать локальную питтинговую коррозию алюминия [3].
Ближе к контакту – больше коррозия
Ускоренная гальваническая коррозия обычно наиболее интенсивна вблизи мест соединения двух металлов; с удалением от мест соединения ее интенсивность уменьшается. Существенное влияние на скорость коррозии оказывает величина отношения площади поверхности катода, контактирующей с электролитом, к площади незащищенной поверхности анода. Желательно иметь малое отношение площади катода к площади анода.
Как избежать гальванической коррозии
- Выбирать в пару алюминию или его сплаву металл, который как можно более ближе к нему в гальваническом ряду для рассматриваемой коррозионной среды (см. рисунок 10).
- Применять «катодный» крепеж. Избегать комбинаций с неблагоприятным (большим) отношением площадей катода к аноду (рисунок 3).
- Обеспечивать полную электрическую изоляцию двух соединяемых металлов. Это может быть выполнено с помощью изолирующих прокладок, втулок, шайб и т.
 п. (рисунок 12).
п. (рисунок 12). - Если применяется окраска, всегда нужно красить катод. Если покрасить только анод, любая царапина на нем даст неблагоприятное отношение поверхностей катода к аноду и приведет к коррозии царапины.
- Увеличивать толщину анода или устанавливать в соединение заменяемые массивные прокладки из анодного металла.
- По возможности размещать гальванический контакт вне коррозионной среды.
- Избегать резьбовых соединений из металлов, образующих гальваническую пару. Заменять их паяными или сварными соединениями.
- Если возможно, применять ингибиторы коррозии, например, в системах с циркуляцией жидкости, которая может играть роль электролита для гальванической коррозии.
- В случаях, когда металлы должны оставаться в электрическом контакте через наружную электрическую цепь, нужно разнести их как можно дальше друг от друга для увеличения сопротивления жидкой цепи (электролита).
- При необходимости и там, где это возможно, применять катодную защиту с цинковым или магниевым жертвенными анодами.

- В наиболее агрессивных средах только цинк, кадмий и магний могут быть в контакте с алюминием без возникновения гальванической коррозии. Заметим, что применение кадмиевых покрытий в значительной степени ограничено из-за их экологической небезопасности.
Рисунок 11 [1]
Рисунок 12 [1]
Источники:
- TALAT 5104.
- Corrosion of Aluminum and Aluminum Alloys. Edited by J.R. Davis. – ASM International, 1999.
- Corrosion of Aluminium / Christian Vargel – ELSEVIER, 2004
- TALAT 1252
Гальваническая
Гальваническая коррозия представляет собой электрохимическую реакцию между двумя и более различными (или разнородными) металлами. Различными, потому что для того, чтобы началась реакция, один должен быть более химически активным (или менее стабильным), чем другой или другие. Когда мы говорим про гальваническую коррозию, то имеем в виду электрообмен. Все металлы обладают электрическим потенциалом, поскольку у всех атомов есть электроны, движение которых и есть электричество.
Все металлы обладают электрическим потенциалом, поскольку у всех атомов есть электроны, движение которых и есть электричество.
Гальваническая коррозия более активного металла начинается в тот момент, когда две или более детали из разнородных металлов, имеющие взаимный контакт (благодаря обычному соприкосновению, или же посредством проводника) помещаются в электролит (любую жидкость, проводящую электричество). Электролитом может быть, что угодно, за исключением химически чистой воды. Не только соленая морская, но и обычная вода из под крана благодаря наличию минеральных веществ является превосходным электролитом, и с ростом температуры электропроводность её только растет (по этой причине корпуса судов, эксплуатирующиеся в жарком климате, заметно больше подвержены коррозии, чем на Севере).
Процесс гальванической коррозии можно наглядно продемонстрировать на примере взаимного контакта изделий из Алюминия и Нержавеющей стали. Алюминий – более химически активный металл является в данном случае анодом, а менее активная нержавеющая сталь – катодом.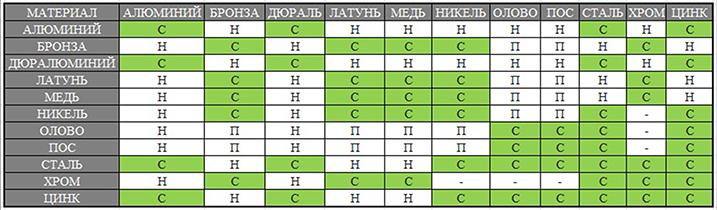 При взаимодействии между нержавеющей сталью и алюминием возникает большая разница потенциалов в соответствии с рядом напряжений в металлах. При этом, благодаря действующему на электрический элемент электролиту (жидкость), возникает электрический ток, и анод, в данном случае Алюминий, корродирует. Подобное явление возникает также в винтовых соединениях, в которых между металлами образуется разность потенциалов, а влажность играет роль электролита.
При взаимодействии между нержавеющей сталью и алюминием возникает большая разница потенциалов в соответствии с рядом напряжений в металлах. При этом, благодаря действующему на электрический элемент электролиту (жидкость), возникает электрический ток, и анод, в данном случае Алюминий, корродирует. Подобное явление возникает также в винтовых соединениях, в которых между металлами образуется разность потенциалов, а влажность играет роль электролита.
Химический ряд напряжений в металлах
| Углерод Платина Золото Серебро Нержавеющая сталь Никель Медь Латунь Олово Свинец Углеродистая сталь Кадмий Алюминий Цинк (оцинкованная сталь) Магний |
Меньшая активность Большая активность |
Чем дальше находятся в ряду напряжений металлы по отношению друг к другу, тем больше разность потенциалов и выше опасность коррозии.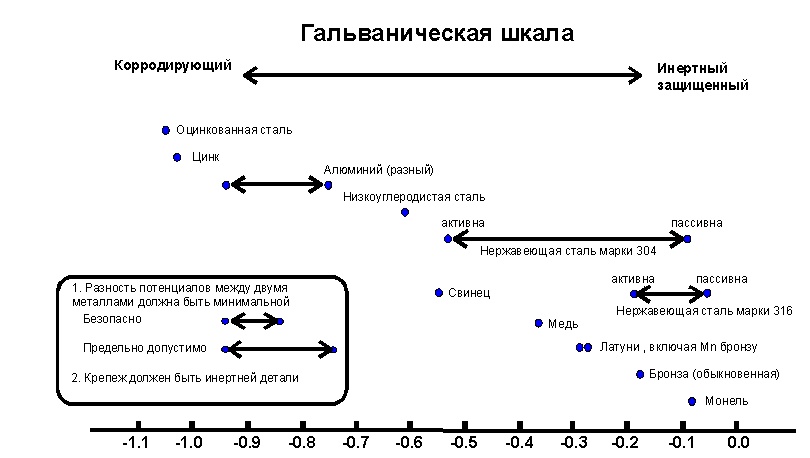 При наличии электролита на большинстве однородных металлических поверхностях все равно образуются крошечные аноды и катоды – в тех местах, где состав сплава неоднороден или имеются вкрапления и примеси – например, частицы металла с форм или штампов.
При наличии электролита на большинстве однородных металлических поверхностях все равно образуются крошечные аноды и катоды – в тех местах, где состав сплава неоднороден или имеются вкрапления и примеси – например, частицы металла с форм или штампов.
Другим важным фктором, оказывающим влияние на скорость протекания гальванической коррозии, помимо разности потенциалов металлов, является пропорциональное соотношение размеров анода и катода. Если к очень большому аноду подключить маленький катод, процесс коррозии анода пойдет медленно. А если поступить наоборот, то анод очень быстро разрушится. Объясняется это тем, что анодные и катодные реакции должны быть эквивалентны. Рост или снижение катодной реакции, обусловленной размером катода, вызывает ответные рост или снижение анодной реакции
Гальваническая коррозия возникает в том случае, если имеет место один из следующих факторов:
- Относительная влажность воздуха превышает 60%;
- Загрязненный воздух: большое количество металлических частиц;
- Металлы в винтовых соединениях, у которых большая разница потенциалов;
- Неправильное соотношение площадей поверхностей анода и катода.

Рекомендации по противодействию гальванической коррозии:
1. Исключите возможность образования гальванического элемента
- защищайте конструкции от действия влажности (удалите электролит)
- изолируйте металлы друг от друга, например, с помощью покрытия
- изолируйте металлы от электролита.
2. Избегайте соединения металлов, у которых большая разница потенциалов.
3. Материал из которого произведен крепеж должен быть более активным (анод), чем материал конструкции (катод).
- площадь поверхности конструкции(катода) больше площади поверхности крепежа(анода).
|
« НазадКоррозия и гальваническая пара 08.11.2011 06:55
Металлы в виду своего разнородного характера не всегда подходят для непосредственного контакта друг с другом тем более, если они находятся в агрессивных средах. Слово «коррозия» заимствованно от латинского слова «corrodere», что означает — пожирать, изгладывать. Наиболее известная форма коррозии, это физико-химической реакция окружающей среды со сталью, которая приводит к появлению ржавчины. Аналогичные процессы проистекают и с другими материалами. Коррозия может быть химической и электрохимической в зависимости от вида процесса разрушения. Химическая коррозия, как правило, вызвана воздействием на сталь сухих газов и жидкостей без электролитных свойств и не сопровождается возникновениями электрических токов. При таком виде коррозии происходит равномерное воздействие на всю поверхность металла, в результате чего появляются окислы в виде рыхлых образований. Химическая коррозия представляет менее опасный вид разрушающих воздействий, в отличие от электрохимической коррозии. Коррозия, при которой происходит возникновение электрического тока, в среде жидкого электролита называется — электрохимическая коррозия. Все металлы и сплавы обладают электрическим потенциалом, из-за наличия в составе сплавов тех или иных веществ их потенциал не однороден. Если взять два материала с разными потенциалами и соединить их между собой, то они образовывают гальваническую пару. Поместив такую связку в электролит, между ними начинается активный электрообмен, что приводит к ускоренному разрушению более активного материала. Электролит, это вещество в среде которого, возможно протекание электрического тока. В качестве электролита может быть не только морская вода, но и обычная водопроводная вода, так как в ней присутствуют минеральные вещества. Коррозионное разрушение алюминиевых частей водной техники, приобретает ускоренный характер, если применять детали из нержавеющей стали в качестве дополнительных элементов. В состав сплава этой легированной стали входят такие вещества как никель и хром, которые не совместимы с алюминием. Какие материалы можно применять для совместного использования без образования гальванической пары можно посмотреть в таблице совместимости металлов и сплавов. К примеру, если металлические детали будет контактировать с деталями на медной основе, процесс разрушения металлических изделий в таком случае резко ускорится. Иногда для защиты стали от коррозии применяют покрытие из слоя олова, но оно будет выполнять свои защитные функции до тех пор, пока не нарушится их целостность. В результате механического воздействия оголяется поверхность материала находившегося под защищающим его слоем, что приводит к образованию гальванической пары олово-железо. Сталь в данном месте будет разрушаться очень быстро. При проведении ремонтных работ нужно учитывать особенности материалов закрепляя их на основное изделие. Замена деталей, не предусмотренных конструкцией, может привести к их преждевременному разрушению и выходу из строя, а в некоторых случаях может повлечь возникновение аварийных ситуаций опасных для жизни. Вот некоторые комбинации несовместимых материалов и сплавов, которые создают гальваническую пару: Алюминий, а так же его сплавы не совместимы с такими материалами как, — медь, сплавы меди, серебро, золото, платина, палладий, родий, олово, никель, хром. Магниево-алюминиевые сплавы при их соединении создают отрицательное взаимодействие с веществами такими как, — никель, хром, олово, медь, свинец, палладий, родий, серебро, золото, платина. Цинк и сплавы на его основе по своей природе не совместимы с медью, славами на основе меди, а так же с некоторыми веществами, например: серебро, золото, платина, палладий, родий. Нелегированная сталь, олово, свинец, кадмий, не совместимы с веществами перечисленными далее: медь, серебро, золото, платина, палладий, родий. Никель и хром, если соединить их с серебром, золотом, платиной, палладием, родием, могут привести к не желательному взаимодействию. |
Цинк, спасающий железо — журнал «АБС-авто»
Немного теории
Как «работает» электрохимическая коррозия? Давайте вспомним азы. Есть в химии такое понятие – электрохимический ряд напряжений металлов. Смотрим на рисунок: литий, калий, …алюминий, цинк, хром, железо, никель, олово, …серебро, платина, золото. Слева расположены более активные металлы, справа – менее активные.
Есть в химии такое понятие – электрохимический ряд напряжений металлов. Смотрим на рисунок: литий, калий, …алюминий, цинк, хром, железо, никель, олово, …серебро, платина, золото. Слева расположены более активные металлы, справа – менее активные.
Если в какой-либо детали имеется соединение двух металлов с различными потенциалами, то в присутствии электролита они образуют гальваническую пару. И чем дальше разнесены металлы в ряду напряжений, тем больше гальванический ток и соответственно сильнее разрушения активного металла. Разрушаясь, он препятствует коррозионному поражению менее активного соседа.
Проиллюстрируем сказанное простым примером. Положим, в стальной автомобильной панели появилась медная заклепка. Медь менее активна, значит коррозионное разрушение железа в месте соединения обеспечено. А если заклепка алюминиевая, картина меняется: разрушаться будет алюминий.
Еще пример. Если покрыть кузовную панель оловом, сначала все будет хорошо. Олово создает пассивный защитный слой, не допуская к стали (железу) влагу и соли. Но когда защитный слой получает повреждение, картина меняется. Между сталью (железом) и оловом мгновенно возникает гальваническая пара. А поскольку олово является менее активным металлом, сталь под воздействием гальванического тока начинает разрушаться.
Но когда защитный слой получает повреждение, картина меняется. Между сталью (железом) и оловом мгновенно возникает гальваническая пара. А поскольку олово является менее активным металлом, сталь под воздействием гальванического тока начинает разрушаться.
Вспомним судьбу консервных банок, изготовленных из луженой жести. Все бывает хорошо, пока банку не поцарапаешь. А уж коль случилось такое, «всей птичке пропасть»: луженая сталь в месте повреждения ржавеет гораздо быстрее нелуженой.
Иная картина с цинком. Защищающий металл (цинк) в ряду напряжений расположен левее железа. Следовательно, и коррозия в поврежденном месте протекает иначе, чем в случае с оловом. Гальваническая пара тоже возникает, но разрушается уже не сталь, а цинк. Но разрушается он очень медленно, сохраняя сталь (железо) на долгие-долгие годы.
Применяется ли это свойство цинка на практике? Конечно, и довольно давно. Но технологии оцинковки непрерывно совершенствуются.
В роли секьюрити
Человечество неплохо научилось бороться с коррозией металла.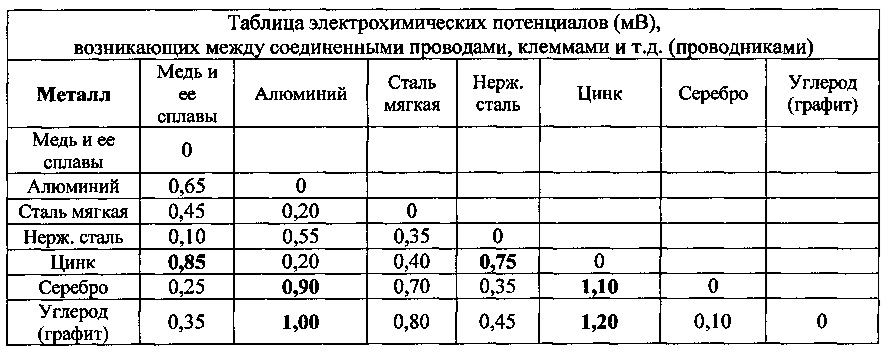 Причем под лозунгом «бей врага его же оружием». Или «лечи подобное подобным» – как вам больше нравится. Например, кузова большинства современных автомобилей оцинковывают на заводах. Покрытие толщиной от 2 до 10 мкм обеспечивает прекрасную защиту от возникновения и распространения коррозионных поражений.
Причем под лозунгом «бей врага его же оружием». Или «лечи подобное подобным» – как вам больше нравится. Например, кузова большинства современных автомобилей оцинковывают на заводах. Покрытие толщиной от 2 до 10 мкм обеспечивает прекрасную защиту от возникновения и распространения коррозионных поражений.
Однако промышленные методы оцинковки – будь то горячее окунание или гальваностегия – не применимы в сервисных и гаражных условиях. Поэтому появление так называемых препаратов холодного цинкования оказалось для ремонтников весьма кстати. Наносимые подобно грунтовке или краске, эти материалы обеспечивают стальной поверхности двойную защиту: активную, как у горячей оцинковки, и пассивную, как у лакокрасочного слоя.
Давайте познакомимся с ними на примере препаратов Dinitrol 443 и Dinitrol 444, выпускаемых шведским химическим концерном DInol AB.
«Характер нордический»
В препаратах Dinitrol 443 содержится 95% химически чистого цинкаЭти препараты представляют собой готовые к применению жидкие однокомпонентные составы, содержащие технически чистый гальванический цинк. «Технически чистый» означает 99,995% Zn, что является очень высоким показателем для промышленного продукта. И вот такого, практически не содержащего примесей, цинка в препаратах Dinitrol 443 и Dinitrol 444 ни много ни мало – 95%. Остальные 5% приходятся на синтетические смолы, безопасный растворитель и некоторые специальные добавки.
«Технически чистый» означает 99,995% Zn, что является очень высоким показателем для промышленного продукта. И вот такого, практически не содержащего примесей, цинка в препаратах Dinitrol 443 и Dinitrol 444 ни много ни мало – 95%. Остальные 5% приходятся на синтетические смолы, безопасный растворитель и некоторые специальные добавки.
Химики знают, что пороговая величина для активизации электрохимического цинкового щита – 92%, а тут все 95! Значит, при прочих равных условиях, пленку материала можно сделать тоньше, а материала потратить меньше – и это тоже относится к заслугам шведских технологий.
Нельзя не сказать и о размерах цинковых частиц – они ограничиваются величиной 3,5 мкм. Искушенные читатели вправе задать естественный вопрос: «А частицы цинка не слипнутся?» Действительно, любая суспензия может потерять однородность. Частицы соберутся в более крупные конгломераты – и прощайте технологические возможности и эксплуатационные козыри.
В препаратах Dinitrol 444 наряду с цинком содержится и диспергированный алюминийЧто сказать на это? Просто суспензия как таковая может преподнести неприятный сюрприз, а вот Dinitrol 443 и Dinitrol 444 – нет.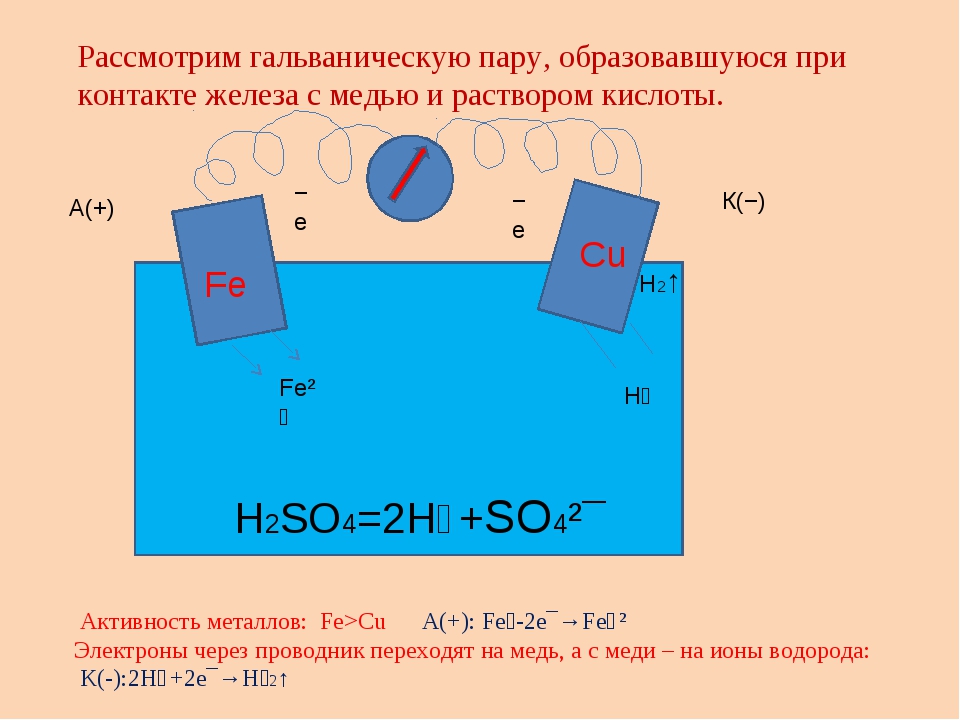 Им помогают те самые специальные добавки, о которых упоминалось выше. Они действуют подобно пептизаторам в коллоидных растворах, поддерживая частицы цинка во взвешенном состоянии и предотвращая их слипание.
Им помогают те самые специальные добавки, о которых упоминалось выше. Они действуют подобно пептизаторам в коллоидных растворах, поддерживая частицы цинка во взвешенном состоянии и предотвращая их слипание.
Очень важна роль синтетической каучуковой смолы, входящей в рецептуру препарата. Благодаря ей слой Dinitrol 443 или 444 обладает отменной адгезией. Но это еще не все: при высыхании он сохраняет эластичность, без проблем выдерживая механические и тепловые деформации.
Кстати, о тепле. А как обстоят дела с термостойкостью? А вот как: пленка препарата выдерживает температуры от –40 до +150 °С без потери эксплуатационных свойств. Так что добро пожаловать и в Сибирь, и в окрасочно-сушильную камеру!
Что касается стойкости к химической агрессии, то «шведы» могут находиться в среде с рН от 5 до 10. Для тех, кто химию подзабыл, напомним: дистиллированная вода имеет рН = 7. Значит, Dinitrol 443 и 444 выдерживает как щелочную, так и кислотную «баню».
Важно знать, что скорость разрушения активного цинкового слоя составляет от 1 до 6 мкм в год. Это гарантирует сохранность защиты в течение 25–50 лет в зависимости от толщины пленки и условий окружающей среды. Словом, на автомобильный век хватит.
Это гарантирует сохранность защиты в течение 25–50 лет в зависимости от толщины пленки и условий окружающей среды. Словом, на автомобильный век хватит.
Как наносим?
«Холодный цинк» марки Dinitrol можно наносить методом воздушного или безвоздушного распыления, кистью, валиком или окунанием.
В фирменной документации говорится, что нанесение препаратов не требует высокой квалификации работника. Это действительно так, особенно если воспользоваться аэрозольным баллончиком. А вот подготовка поверхности требует тщательности и профессионализма. Главное – обеспечить требуемую чистоту и шероховатость.
Говорите, стальные диски ржавеют? Теперь не будут.И это лишь одно из многих применений «холодного цинка» DinitrolПрепарат можно наносить на вертикальные и наклонные поверхности. Важно добиваться ровного слоя, без подтеков и пузырей. При толщине пленки 40 мкм расход составит 0,25 кг/м2. Высыхание длится 48 ч при комнатной температуре (на отлип – 10 мин). Для ускорения сушки деталь можно поместить в камеру и выдержать 30–60 мин при 60 °С. Повторный слой материала наносится через час. Полученную пленку можно окрашивать практически всеми видами ЛКМ.
Повторный слой материала наносится через час. Полученную пленку можно окрашивать практически всеми видами ЛКМ.
И в заключение отметим, что области применения новых шведских препаратов весьма обширны: автомобильный и другой транспорт, мосты, дороги, тоннели, строительные конструкции, промышленные и городские объекты, гидросооружения, нефтегазовая промышленность. Так что не автосервисом единым… Материалы Dinitrol 443 и Dinitrol 444 пригодятся во многих сферах человеческой деятельности.
Как совместить несовместимое (о коррозии металлов)
Разнородные металлы при их непосредственном контакте «выносят» друг друга далеко не всегда. Нередко они образуют довольно сильную гальваническую пару, что приводит к коррозии одного из контактирующих металлов, а иногда и к «схватыванию» этого соединения, делая невозможной его последующую разборку для ремонта.
На память приходит случай из собственной практики, когда я, еще будучи молодым инженером, работал на автогиганте. Мы доводили новую систему автомобиля — экономайзер с электронным управлением. И столкнулись с тем, что после некоторого пробега машины входящие в систему электромагнитные клапаны, покрытые никелем, наотрез отказывались выворачиваться из своих гнезд. А снимать клапаны приходилось довольно часто — для проверки. Если же их вывинчивали «насильно», они выходили «с мясом» — вся резьба клапанов была сплошняком покрыта алюминием, выдранным из смесительной камеры карбюратора.
Мы доводили новую систему автомобиля — экономайзер с электронным управлением. И столкнулись с тем, что после некоторого пробега машины входящие в систему электромагнитные клапаны, покрытые никелем, наотрез отказывались выворачиваться из своих гнезд. А снимать клапаны приходилось довольно часто — для проверки. Если же их вывинчивали «насильно», они выходили «с мясом» — вся резьба клапанов была сплошняком покрыта алюминием, выдранным из смесительной камеры карбюратора.
Чтобы избежать подобной неприятности, резьбу смазывали, в том числе и графитовой смазкой, но ничто не помогало. Попробовали было заменить никелевое покрытие клапанов на кадмиевое, но тогда клапаны засели и вовсе «намертво». Чтобы их вывернуть, обычного полуметрового динамометрического ключа (до 10 кгс) уже не хватало — пришлось орудовать ломом. Правда, покрытая кадмием резьба теперь выходила из камеры без привычной алюминиевой корки. Дефект устранялся, если на резьбу наносили слой цинка. Но цинк нас тоже не устраивал. Покрытие из него нестойкое, оно быстро истиралось и вода, всегда содержащаяся в бензине, вызывала ржавление клапанов, которые просто переставали действовать.
Покрытие из него нестойкое, оно быстро истиралось и вода, всегда содержащаяся в бензине, вызывала ржавление клапанов, которые просто переставали действовать.
Лишь применив комбинированное покрытие «хром по никелю», мы навсегда избавились от этого дефекта. (Никель по-прежнему был нужен, поскольку хром не хотел ложиться на металл клапана.)
Обратившись уже после к таблице совместимости металлов (она тогда была почему-то секретной!), мы убедились, что наш чисто эмпирический выбор был сделан правильно. Жаль только, что из-за элементарной неразберихи так много времени было тогда убито впустую. Вот если бы эта «секретная» табличка была бы у нас тогда под рукой…
На таблице 1 эти «секретные» данные представлены в сокращенном виде. Из нее видно, что алюминий вполне может контактировать с цинком и хромом (знак +). А вот контакт с никелем ему противопоказан (знак -). Графу с кадмием я не привожу потому, что кадмирование сейчас почти повсеместно отменено из-за канцерогенности этого процесса.
Таблица 1. Гальваническая совместимость металлов
Анализ таблицы 1 показывает, что медь и ее сплавы (латуни и бронзы), алюминий и его сплавы (дюрали), а также олово и его сплавы (припои ПОС) ведут себя синхронно. Значит, эту таблицу можно упростить (см. таблицу 2).
Таблица 2. Упрощенный вид таблицы 1
Это упрощение облегчает пользование таблицей. Но все равно это не решает проблемы в полной мере. Ведь запоминать наизусть, словно «долбицу умножения», столь громоздкую таблицу (состоящую из 49 клеток) вряд ли кто будет. А каждый раз разыскивать таблицу, прежде чем приладить одну деталь к другой, никакой любитель мастерить тоже не будет. Как же быть?
Попробуем переложить таблицу 2 на ряд формальных (мнемонических) фраз, а именно:
1. Сталь (нелигированная!) не любит медь.
2. Алюминий не любит медь и никель, а с оловом его нужно обязательно паять (буква П).
3. Медь не любит сталь, алюминий и цинк, а с оловом ее нужно паять.
4. Хром любит всех, а с оловом нуждается в пайке.
5. Никель не любит алюминий, а с оловом его нужно паять.
6. Цинк не любит медь.
7. Олово любит сталь и цинк, а с остальными — пайку.
Можно заметить, что 6-е высказывание лишнее. Ведь в 3-м высказывании уже содержится «нелюбовь» меди к цинку, а односторонней любви среди металлов не может быть (во всяком случае, мы будем так условно считать). Значит, 3-е высказывание отбрасывать уже нельзя. Затем, 1-е высказывание оказывается лишним: «нелюбовь» стали и меди следует из 3-го высказывания. Далее, 7-е высказывание тоже, видимо, требуется сохранить. Тогда 4-е высказывание будет лишним — слова «с оловом нуждается в пайке» косвенным образом содержатся в 7-м высказывании. Потом, 2-е высказывание тоже требует сохранения, вот только слова «а с оловом его нужно паять» лишние (это и так ясно из 7-го высказывания). Наконец, в 3-м высказывании слово «алюминий» лишнее: «нелюбовь» меди и алюминия уже содержатся во 2-м высказывании. Дальше минимизировать нам уже нечего.
Дальше минимизировать нам уже нечего.
Таким образом, после ряда упрощений мы получили уже не семь, а всего лишь три высказывания:
1. Алюминий не любит никель и медь.
2. Медь не любит сталь и цинк.
3. Олово любит сталь и цинк, с остальными — пайку.
Как стихотворение, эти простые фразы запомнит едва ли не каждый. Они помогут вам правильно ориентироваться при работе с металлом, даже не имея под рукой никакой таблицы.
2-я фраза наиболее показательна: смоченная обычной водой медь беспощадно разрушает сталь и цинк. Помирить их сможет, например, облуживание «агрессивной» меди (полуда не страшна ни стали, ни цинку). «Агрессия» меди распространяется и на алюминий. Спасти последний может лужение меди, а также ее цинкование и хромирование, но не никелирование. Хотя облудить разрешается и алюминий, благо рецептов этой операции сейчас существует уже немало. Спасет лужение алюминий и от «агрессии» со стороны никеля. Следовательно, все конфликты, содержащиеся в 1-й и 2-й фразах, мы разрешили. Ну а к 3-й фразе комментарии, как говорится, излишни.
Ну а к 3-й фразе комментарии, как говорится, излишни.
Откуда известно, какой металл пострадает в нежелательной (или, наоборот, нужной нам) гальванической паре? А из ряда активности металлов. Воспроизведем его частично: Аl, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, Cu. Этот ряд показывает, что алюминий (AI) тут наименее активный металл, то есть самый слабый, а медь (Си), наоборот, наиболее активный металл, то есть она самая сильная. Поэтому в паре, скажем, железо (Fe) и медь (Cu) безусловным победителем окажется медь, то есть разрушаться будет только железо.
Поэтому непременно нужно сказать, что все плюсы и минусы, указанные в таблицах, весьма условны. Любые два разнородных металла образуют гальваническую пару. Только в одних случаях она «сильная», а в других «слабая». К примеру, таблица говорит о допустимости контакта олова (полуды) и стали. Однако попробуйте закопать в землю вскрытую консервную банку. Вскоре от нее останется одна ржавчина с остатками полуды. Влага, а главное соли, приведут к тому, что когда-то защитный слой полуды теперь неизбежно разрушит жесть. Вот если бы контакт полуды и жести не был бы открыт (то есть банка была бы цела), этого бы не произошло.
Вот если бы контакт полуды и жести не был бы открыт (то есть банка была бы цела), этого бы не произошло.
То же самое можно сказать и контакте стали и цинка. Таблица нам рекомендует эту пару. Но вот если это соединение поливать соленой водой, цинк (Zn) будет непременно разрушаться. Именно на этом как раз и обоснована весьма популярная сейчас анодная защита кузова легкового автомобиля.
Цинковую пластинку надежно прикрепляют к кузову (с небольшим зазором, но без электрического контакта с кузовом). Контакт же пластинки с кузовом производится отдельным проводом, идущим от пластинки (провод крепят к кузову на некотором удалении от пластинки).
Когда всегда имеющаяся на асфальте в сырую погоду соленая вода начнет поливать кузов и цинковую пластинку, в зазоре образуется электролит: пара «кузов-пластинка» превратится в элементарную батарейку. При этом ток от этой батарейки начнет течь через упомянутый провод и кузов машины. Цинк, как более «слабый» в гальванопаре «цинк-железо», начнет разрушаться, предохраняя стальной кузов от коррозии.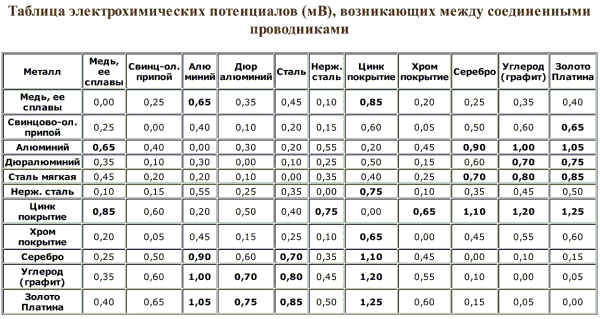 Установите у себя на автомобиле десяток таких пластин — ржавление кузова прекратится.
Установите у себя на автомобиле десяток таких пластин — ржавление кузова прекратится.
Чтобы защитить от коррозии стальную ограду (например, на кладбищенской могиле), достаточно в землю вкопать четыре-пять цинковых пластин, соединив с ними проводом верх ограды. «Батарейкой» (вернее, гальваническим элементом) тут будет сама влажная земля. Такая анодная защита мало чем отличается от автомобильной.
Выходит, «все врут календари», то бишь таблицы. Нет, не врут. Просто они ориентируют нас на обычные условия эксплуатации соединений, когда явной сырости, а тем более соли, нет. Да и в их присутствии урон будет минимальным. Поэтому не поленитесь запомнить найденные нами три предложения. Они помогут вам выполнять свои самоделки грамотно.
Гальванические пары металлов
Обучение и техническая поддержка для проектировщика на Prof-il.ru
Гальванические пары металлов
Атмосферная коррозионная стойкость алюминия обьясняется наличием оксидной пленки, образующейся сразу после взаимодействия металла с кислородом воздуха (Литер. : В.Ф. Хенли «Анодное оксидирование алюминия и его сплавов»).
: В.Ф. Хенли «Анодное оксидирование алюминия и его сплавов»).
Табл. 1 Совместимость металлов и сплавов
С — совместимые
Н — несовместимые
П — совместимые при пайке, но несовместимые при непосредственном соприкосновении, так как образуют гальваническую пару
ПОС — припой оловянно-свинцовый
Сталь — нелегированная
Пример нежелательных гальванических пар:
1 ПАРА: алюминий и все сплавы на его основе не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
— с оловом
— с никелем
— с хромом
2 ПАРА: алюминий и все сплавы на его основе не рекомендуется и недопустимо сочетать:
— с титаном и с его сплавами
3 ПАРА: магниево-алюминиевые сплавы не рекомендуется и недопустимо сочетать:
— с хромом
— со свинцом
— со сталью легированной и нелегированной
— с медью
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
— с оловом
— с никелем
4 ПАРА: цинк и его сплавы не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
5 ПАРА: никель и хром не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
6 ПАРА: сталь нелегированная, олово, свинец, кадмий не рекомендуется и недопустимо сочетать:
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
Рисунок 1 — Гальваническая коррозия двух деталей из разнородных металлов
Гальваническая коррозия более активного металла начинается в тот момент, когда две или более детали из разнородных металлов, имеющие взаимный контакт (благодаря обычному соприкосновению, или же посредством проводника) помещаются в электролит (любую жидкость, проводящую электричество). Электролитом может быть что угодно, за исключением химически чистой воды. Не только соленая морская, но и обычная вода из-под крана благодаря наличию минеральных веществ является превосходным электролитом, и с ростом температуры электропроводность ее только растет.
Электролитом может быть что угодно, за исключением химически чистой воды. Не только соленая морская, но и обычная вода из-под крана благодаря наличию минеральных веществ является превосходным электролитом, и с ростом температуры электропроводность ее только растет.
Катод — электрод, на котором происходит процесс восстановления, а анод — это электрод, где протекают окислительные процессы.
Ряд активности металлов (электрохимический ряд напряжений металлов)
1 — Активные металлы
2 — Металлы средней активности
3 — Неактивные металлы
Химическая коррозия — металлы защищают себя оксидной пленкой на своей поверхности, является ли она самовосстанавливающейся, вот вопрос, как в случае алюминия, нержавеющей стали, цветных металлов или же как у стали отделяется.
© PROF-IL.RU 2016 — | При использовании материалов сайта, пожалуйста, указывайте ссылку https://prof-il. ru | Информация на сайте не является публичной офертой. | Обо всех замеченных ошибках при работе сайта просьба сообщать при помощи формы обратной связи. | Настоящий ресурс может содержать материалы 18+
ru | Информация на сайте не является публичной офертой. | Обо всех замеченных ошибках при работе сайта просьба сообщать при помощи формы обратной связи. | Настоящий ресурс может содержать материалы 18+
Компьютерная версия сайта
| | Навигация по справочнику TehTab.ru: главная страница / / Техническая информация / / Инженерные приемы и понятия / / Защита от воздействия окружающей среды. Коррозия. Климатические исполнения / / Таблица 2 совместимости металлов и сплавов (оценка риска гальванической коррозии).
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Нашли ошибку? Есть дополнения? Напишите нам об этом, указав ссылку на страницу. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| TehTab.ru Реклама, сотрудничество: [email protected] | Обращаем ваше внимание на то, что данный интернет-сайт носит исключительно информационный характер. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Все риски за использование информаци с сайта посетители берут на себя. Проект TehTab.ru является некоммерческим, не поддерживается никакими политическими партиями и иностранными организациями. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Оцинкованная сталь с алюминием… | Американская ассоциация гальванизаторов
Что происходит, когда я соединяю оцинкованную сталь с алюминиевыми деталями или кладу алюминиевые листы на шпильки из оцинкованной стали?
Часто задают вопрос, когда два разнородных металла контактируют друг с другом. На диаграмме ниже показаны электродные потенциалы металлов в морской воде. Если два металла с разными потенциалами контактируют и присутствует проводящая среда, такая как морская вода или конденсат, может произойти реакция, обычно известная как гальванический элемент.
Чем выше разность электрических потенциалов, тем больше вероятность реакции. В случае цинка и алюминия существует лишь небольшая вероятность реакции из-за относительно небольшого изменения потенциала между двумя металлами и образования изолирующей пленки на поверхности алюминия.
Одним из ключевых факторов реакции между разнородными металлами является площадь поверхности контакта. Серьезная реакция может возникнуть, когда большой катод (более высокий или более положительный потенциал) находится в контакте с маленьким анодом (более низкий или отрицательный потенциал).В этой ситуации скорость коррозии может резко возрасти.
Другой ключевой фактор в определении коррозии двух разнородных металлов в присутствии проводящих веществ. Во многих случаях конденсированная вода не обеспечивает достаточной проводимости для начала процесса коррозии. По возможности, лучшим решением для этого типа коррозии является создание изоляционного барьера между двумя разнородными металлами.
Для получения дополнительной информации о горячеоцинкованной стали, контактирующей с разнородными металлами, см. Руководство AGA по разнородным металлам.
Электродные потенциалы металла в морской воде
| Материал | Potentail (вольт) |
|---|---|
| Магний | -1,55 |
| Цинк | -1,10 |
| Алюминий | -0,86 |
| Кадмий | -0,77 |
| Чугун | -0,68 |
| Углеродистая сталь | -0,68 |
| Нержавеющая сталь 18% CR 8% Ni (активный) | -0.61 |
| Свинец | -0,57 |
| Припой (50Pb / 50Sn) | -0,52 |
| Олово | -0,49 |
| Медь | -0,43 |
| Алюминий Бронза | -0,41 |
В контакте с другими металлами
Главная » Горячее цинкование » Как долго действует HDG? » в контакте с другими металлами
Если цинк контактирует с другим металлом, существует возможность коррозии из-за биметаллической пары. Степень коррозии зависит от положения другого металла относительно цинка в гальванической серии и, в меньшей степени, от относительного размера площади поверхности двух соприкасающихся металлов.
Степень коррозии зависит от положения другого металла относительно цинка в гальванической серии и, в меньшей степени, от относительного размера площади поверхности двух соприкасающихся металлов.
Каждый раз, когда биметаллический узел содержит металлические системы, подверженные гальванической коррозии, необходимо тщательно учитывать соотношение площади катода и площади анода. Ток коррозии, протекающий между катодом и анодом, не зависит от площади, но скорость проникновения на анод зависит от тока на единицу площади, то есть плотности тока.Следовательно, нежелательно иметь большую поверхность катода в контакте с небольшой поверхностью анода. Скорость проникновения из-за коррозии увеличивается с увеличением отношения площади поверхности катода к площади анода.
Например, при использовании стального листа без покрытия с цинковой заклепкой отношение площади поверхности катода к площади поверхности анода велико, и заклепка быстро выйдет из строя из-за ускоренной коррозии. При объединении цинковой пластины с заклепкой из нержавеющей стали соотношение площадей между катодом и анодом меняется на обратное, и, хотя это влияет на большую площадь поверхности, глубина проникновения мала; крепеж не должен выходить из строя из-за коррозии.
При объединении цинковой пластины с заклепкой из нержавеющей стали соотношение площадей между катодом и анодом меняется на обратное, и, хотя это влияет на большую площадь поверхности, глубина проникновения мала; крепеж не должен выходить из строя из-за коррозии.
Поведение гальванических покрытий при контакте с различными металлами обобщено в таблице ниже. Приведенная информация предоставляется в качестве руководства, чтобы избежать ситуаций, в которых может возникнуть коррозия при контакте оцинкованных поверхностей с другим металлом.
Следующая информация содержит более подробную информацию о других распространенных металлах, используемых в строительстве, которые могут контактировать со сталью, оцинкованной горячим способом.
Медь и латунь
Если установка требует контакта между оцинкованными материалами и медью или латунью во влажной или влажной среде, может произойти быстрая коррозия цинка.Даже сточные воды с медных или латунных поверхностей могут содержать достаточно растворенной меди, чтобы вызвать быструю коррозию. Если использование меди или латуни в контакте с оцинкованными предметами неизбежно, следует принять меры для предотвращения электрического контакта между двумя металлами. Поверхности стыков следует изолировать непроводящими прокладками; соединения должны производиться с помощью изолирующих крепежных элементов. Конструкция должна обеспечивать отсутствие рециркуляции воды и ее протекание от оцинкованной поверхности к поверхности из меди или латуни, а не наоборот.
Если использование меди или латуни в контакте с оцинкованными предметами неизбежно, следует принять меры для предотвращения электрического контакта между двумя металлами. Поверхности стыков следует изолировать непроводящими прокладками; соединения должны производиться с помощью изолирующих крепежных элементов. Конструкция должна обеспечивать отсутствие рециркуляции воды и ее протекание от оцинкованной поверхности к поверхности из меди или латуни, а не наоборот.
Алюминий и нержавеющая сталь
В атмосферных условиях от умеренной до умеренной влажности контакт между оцинкованной поверхностью и алюминием или нержавеющей сталью вряд ли вызовет существенную дополнительную коррозию. Однако в очень влажных условиях оцинкованной поверхности может потребоваться электрическая изоляция от алюминия или нержавеющей стали.
Погодостойкая сталь
Когда оцинкованные болты используются для атмосферостойкой стали, цинк сначала пожертвует собой, пока на стойкой к атмосферным воздействиям стали не образуется защитный слой ржавчины. Как только этот слой ржавчины образуется, он образует изолирующий слой, который предотвращает дальнейшее разрушительное действие цинка. Цинковое покрытие должно быть достаточно толстым, чтобы прослужить до образования слоя ржавчины, обычно несколько лет. Большинство горячеоцинкованных болтов имеют достаточно цинкового покрытия, чтобы прослужить до тех пор, пока на стали, устойчивой к атмосферным воздействиям, не образуется защитный слой ржавчины, с минимальной потерей срока службы покрытия.
Как только этот слой ржавчины образуется, он образует изолирующий слой, который предотвращает дальнейшее разрушительное действие цинка. Цинковое покрытие должно быть достаточно толстым, чтобы прослужить до образования слоя ржавчины, обычно несколько лет. Большинство горячеоцинкованных болтов имеют достаточно цинкового покрытия, чтобы прослужить до тех пор, пока на стали, устойчивой к атмосферным воздействиям, не образуется защитный слой ржавчины, с минимальной потерей срока службы покрытия.
| Окружающая среда | ||||||
|---|---|---|---|---|---|---|
| Атмосферное | Погруженное | |||||
| Металл в контакте | Сельское хозяйство | Промышленное / Городское | Морское | Пресное Вода | 20 Море Вода | 20 Море |
| Алюминий и алюминиевые сплавы | 0 | 0 до 1 | 0 до 1 | 1 | 2 до 3 | |
| Алюминиевая бронза и кремниевая бронза | 0 до 1 | 1 | 1 до 2 | 1 до 2 | 2 до 3 | |
| Латунь, включая высокопрочная (HT) латунь (марганцевая бронза) | 0 до 1 | 1 | 0 до 2 | 1 до 2 | 2 до 3 | |
| Кадмий | 0 | 0 | 0 | 0 | 0 | |
| Чугун | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 1 до 3 | |
| Чугун (аустенитный) | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Хром | от 0 до 1 | от 1 до 2 | от 1 до 2 | от 1 до 2 | 2 до 3 | |
| Медь | от 0 до 1 | от 1 до 2 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Медно-никель | 0 до 1 | от 0 до 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Золото | (от 0 до 1) | (от 1 до 2) | (от 1 до 2) | (От 1 до 2) | (от 2 до 3) | |
| Металлы, фосфорная бронза и зубчатая бронза | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Свинец | от 0 до 1 | от 0 до 1 | от 0 до 1 | от 0 до 2 | (от 0 до 2) | |
| Магний и магниевые сплавы | 0 | 0 | 0 | 0 | 0 | |
| Никель | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Никелево-медные сплавы | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Никель-хром-железные сплавы | (от 0 до 1) | (1) | (от 1 до 2) | 90 027 (от 1 до 2)(от 1 до 3) | ||
| Никель-хром-молибденовые сплавы | (от 0 до 1) | (1) | (от 1 до 2) | (от 1 до 2) | (от 1 до 3) | |
| Никелевый серебристый | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 1 до 3 | |
| Платина | (от 0 до 1) | ( От 1 до 2) | (от 1 до 2) | (от 1 до 2) | (от 2 до 3) | |
| Родий | (от 0 до 1) | (от 1 до 2) | (от 1 до 2 ) | (от 1 до 2) | (от 2 до 3) | |
| Серебро | (от 0 до 1) | (от 1 до 2) | (от 1 до 2) | (от 1 до 2) | (От 2 до 3) | |
| Твердый припой | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 2 до 3 | |
| Припои мягкие | 0 | 0 | 0 | 0 | ||
| Нержавеющая сталь (аустенитные и другие марки, содержащие примерно 13% хрома) | От 0 до 1 | от 0 до 1 | от 0 до 1 | от 0 до 2 | от 1 до 2 | |
| Нержавеющая сталь (мартенситные марки, содержащие приблизительно 13% хрома) | 0 до 1 | 0 до 1 | От 0 до 1 | от 0 до 2 | от 1 до 2 | |
| Стали (углеродистые и низколегированные) | от 0 до 1 | 1 | от 1 до 2 | от 1 до 2 | от 1 до 2 | |
| Олово | 0 | от 0 до 1 | 1 | 1 | от 1 до 2 | |
| Титан и титановые сплавы | (от 0 до 1) | (1) | (от 1 до 2) | (от 0 до 2) | (от 1 до 3) | |
Ключ:
Общие примечания: Рейтинги в скобках основаны на очень ограниченных доказательствах и, следовательно, менее достоверны, чем другие указанные значения.Таблица относится к дополнительной коррозии, и символ «0» не следует понимать как означающий, что контактирующие металлы не нуждаются в защите при любых условиях воздействия. Источник: Британский институт стандартов, стр. 6484: 1979, таблица 23 | ||||||
Просмотрите эту диаграмму в формате PDF
Гальваническая коррозия между оцинкованной сталью и алюминием
Образование, Алоха и самое интересное
можно в отделке металлом
Добро пожаловать на самый популярный и авторитетный в мире веб-сайт по отделке металлов
тема 41930 Обсуждение началось в
2006 г. , но продолжаются до 2019 г.
, но продолжаются до 2019 г.
В.В баскетбольном зале устанавливаем скамейки из анодированного алюминия. Поставщик предоставил кронштейны из оцинкованной стали для крепления к скамейке и оцинкованные стальные болты для крепления кронштейна к бетону.
Вопросы:
1) Достаточно ли оцинкованного кронштейна для предотвращения коррозионного взаимодействия между сталью и алюминием?
2) Прикрепив стальной кронштейн непосредственно к бетону, обеспечит ли это достаточное заземление для предотвращения электролиза?
— Хантингтон-Бич, Калифорния,
2006 г.
А.Привет, Рональд. Насколько мне известно, заземление не ускоряет и не замедляет гальваническое действие; Я думаю, что эта часть не имеет значения, пока вы не вводите дополнительные материалы.
Ячейку гальванической коррозии для простоты понимания можно сравнить с сухой батареей:
— Два металла в вашей конструкции (алюминий и цинк) действуют как углерод и цинк в батарее, а их разница в электрохимическом потенциале обеспечивает движущая сила. В зависимости от конкретного алюминиевого сплава эта разность потенциалов между ним и цинком может составлять около 0.2 вольта, а не 1,5 вольта разности потенциалов между углеродом и цинком.
В зависимости от конкретного алюминиевого сплава эта разность потенциалов между ним и цинком может составлять около 0.2 вольта, а не 1,5 вольта разности потенциалов между углеродом и цинком.
— Окружающая влага и скопившиеся соли играют роль проводящей глотки в батарее. Если для очистки не используется отбеливатель, или в других необычных обстоятельствах, окружающая среда, вероятно, будет довольно сухой и непроводящей.
— Физическое соединение двух металлов без изоляторов между ними похоже на соединение положительного и отрицательного полюсов батареи с помощью провода. Когда целесообразно использовать изоляторы, следует использовать их, и тогда гальваническая коррозия исключена.
Я видел несколько похожую конструкцию на то, о чем вы говорите, — оцинкованная сталь и анодированный алюминий — без проблем использовались при строительстве на открытом воздухе, пока находились вдали от моря, поэтому при использовании внутри помещений это должно быть еще меньше. Вероятно, это связано с тем, что цинк и алюминий довольно близки гальванически, а анодированный алюминий имеет непроводящую анодированную пленку на нем, которая ограничивает контакт металла с металлом. Но там, где я это видел, гальванизированные U-образные болты прикреплены к алюминию, поэтому анодированная пленка была меньше разрушена, чем если бы вы сверлили ее, обнажая голый алюминий, и скручивали ее.Но если болты большие, я бы использовал оцинкованные, а не оцинкованные болты; и если они маленькие (и, следовательно, доступные), я бы использовал болты из нержавеющей стали.
Но там, где я это видел, гальванизированные U-образные болты прикреплены к алюминию, поэтому анодированная пленка была меньше разрушена, чем если бы вы сверлили ее, обнажая голый алюминий, и скручивали ее.Но если болты большие, я бы использовал оцинкованные, а не оцинкованные болты; и если они маленькие (и, следовательно, доступные), я бы использовал болты из нержавеющей стали.
Также важно понимать, что «достаточно хорошо» всегда зависит от обстоятельств. Оцинкованные болты на алюминиевых трибунах — это одно, и, вероятно, это нормально, особенно в помещении, но оцинкованные болты абсолютно не могут использоваться для соединения алюминиевых деталей самолетов. Удачи.
Тед Муни, P.E.
отделка.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
2006 г.
A. Я согласен с мистером Муни. В таких внутренних помещениях, как это, оцинкованное и оцинкованное оборудование не должно представлять реальной угрозы. Однако, если вы хотите сделать еще один шаг, чтобы гарантировать, что гальваническая коррозия не будет проблемой, я рекомендую обратить внимание на покрытия из дисперсии цинка / алюминия. Эти тонкие сухие пленочные покрытия защищают сталь от красной ржавчины, одновременно рассеивая биметаллические ячейки, образующиеся при контакте стальной арматуры с алюминием.
Эти тонкие сухие пленочные покрытия защищают сталь от красной ржавчины, одновременно рассеивая биметаллические ячейки, образующиеся при контакте стальной арматуры с алюминием.
— Кливленд, Теннесси
2006
В. Я понимаю аккумуляторные аспекты гальванического взаимодействия разнородных металлов. Что касается заземления, я думал о заземлении, которое используется в микроволновых башнях и проводах, прикрепленных к медному заземлению. Интересно, даст ли заземление скамейке дорогу току вместо того, чтобы жертвовать металлом. Целью было бы осуществить взаимодействие между оцинкованной сталью и почвой. Отводы на башнях будут иметь больше паразитных токов.
Я уверен, что анодированная поверхность обеспечит достаточную изоляцию.
консультант — Хантингтон-Бич, Калифорния
А. Привет, Рональд.
Различные типы систем заземляются по разным причинам, не обязательно для предотвращения гальванической коррозии. Но вы можете взять автомобильный аккумулятор и заземлить любой полюс (но не оба), не влияя на его работу, и я думаю, что то же самое можно сказать и о гальванической батарее.
Но вы можете взять автомобильный аккумулятор и заземлить любой полюс (но не оба), не влияя на его работу, и я думаю, что то же самое можно сказать и о гальванической батарее.
С уважением,
Тед Муни, П.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
2007
В. У меня новый 5-колесный внедорожник с алюминиевыми оконными рамами. Винты, удерживающие окна, начали ржаветь, и теперь из разных участков рельсового пути, по которому скользит окно, появляется кристаллический рост. Некоторые винты буквально развалились. У меня также пропадает питание от моих двенадцатавольтных батарей. Может ли этот электролиз быть вызван заземлением электрической цепи или, скорее всего, вызван контактом с проводом под напряжением, возможно, винтом, пробивающим провод под напряжением?
Lyle A BalfourConsumer — Ревелсток, Британская Колумбия, Канада
Алюминиевая теплица на оцинкованной нижней части
18 мая 2009 г.
В.Мне нужно установить теплицу с алюминиевыми стенками, и мой вопрос: могу ли я установить нижние колонтитулы из оцинкованной стали и прикрутить алюминиевый сайдинг непосредственно к нижним колонтитулам, не беспокоясь о коррозии? Есть ли лучший способ установить эту связь?
Leslie Fayювелир / мастер по металлу — silver spring, Мэриленд
20 мая 2009 г.
А. Крепление алюминиевого сайдинга к стали следует производить неметаллическими [ред. примечание: т. е. изолированные] крепежные детали из нержавеющей стали или крепежные детали класса 5 со специальным покрытием для предотвращения не только нормальной коррозии крепежа, но и явления, называемого коррозией под действием водорода при растрескивании под напряжением.Вы также можете подумать об использовании изолятора между алюминием и сталью, он послужит двойной цели — термическому разделению, если вы решите изолировать стену и кондиционировать замкнутое пространство. Вы не сказали, оцинкована ли сталь или какой должна быть отделка алюминия. Все это имеет значение для ответа.
Все это имеет значение для ответа.
— Кантон, Коннектикут
Каркасы тентов из смешанной алюминиевой и оцинкованной конструкции
10 мая 2011 г.В. Я хочу заменить оцинкованные рамы и фурнитуру для палаток на алюминий.Я не смогу сделать их все сразу, есть ли опасность смешать оцинкованные детали с алюминиевыми опорами за это время? Палатки подвержены воздействию солнца и дождя.
Кроме того, фитинги из ПВХ были бы прочными и достаточно прочными, чтобы их можно было использовать с алюминиевыми опорами для создания рам, выдерживающих до 30 фунтов, разбросанных по площади 100–125 квадратных футов.
Trice Ray— Бриджтаун, Барбадос
12 мая 2011 г.
А. Привет, Трайс.
Я не могу ответить на вопрос о фитингах из ПВХ, и у меня нет четкого представления о том, о чем вы спрашиваете, но, возможно, другой читатель ответит.
Каждый раз, когда два разных металла действительно касаются друг друга (контакт металл-металл) во влажной среде, возникает некоторая вероятность гальванической коррозии. Однако серьезность ситуации сильно варьируется и зависит от приложения. Например, в авиалайнере это было бы совершенно недопустимо. Но я видел, как оцинкованные и алюминиевые перила и фурнитура смешивались во многих случаях без серьезных последствий; Я был бы очень удивлен, если бы при соприкосновении полюсов возникла гальваническая коррозия; если они не соприкасаются, вы не можете.Удачи.
Однако серьезность ситуации сильно варьируется и зависит от приложения. Например, в авиалайнере это было бы совершенно недопустимо. Но я видел, как оцинкованные и алюминиевые перила и фурнитура смешивались во многих случаях без серьезных последствий; Я был бы очень удивлен, если бы при соприкосновении полюсов возникла гальваническая коррозия; если они не соприкасаются, вы не можете.Удачи.
С уважением,
Тед Муни, P.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
Электролиз между алюминиевыми солнечными панелями и оцинкованными каркасами
2002 г.В. Произойдет ли электролиз при контакте алюминия с оцинкованной сталью?
Craig Hornerсолнечная энергия — Чико, Калифорния
2002
A. Да, хотя алюминий и цинк (гальваническое покрытие) довольно близко друг к другу по электрохимической активности в ряду морской воды, они недостаточно близки.Гальваническая совместимость с алюминием — одна из причин, благодаря которой кадмий так долго сохранялся, несмотря на его токсичность.
Истинная совместимость достигается за счет цинкования или всего алюминия, но хорошее анодирование алюминия очень поможет. Вопрос в размере 64000 долларов, конечно же, заключается в том, каковы детали заявки?
Тед Муни, P.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
15 марта 2012
В. Я хотел бы задать вопрос о солнечных батареях.Обычно мы делаем солнечную установку с расчетным сроком службы 25 лет; В настоящее время мы используем панели с алюминиевым каркасом и «оцинкованный» каркас, покрытый горячим цинком, для крепления панелей с помощью болтов из нержавеющей стали. На мой вопрос, конечно, идет немного кислоты в дождь, и здесь идет довольно много дождя, а также, помимо заводов, можно ожидать других загрязняющих веществ, вызывающих коррозию.
Что бы порекомендовать при продолжительности жизни 25 лет? Нейлоновые прокладки для разделения панелей и рамы? Или есть материалы получше? Или это не будет проблемой?
Спасибо за уделенное время!
Солнечные панели Arjen Helder— Сямэнь, Китай
25 августа 2010 г.
В.Привет,
Мы производим стеллажи для солнечных батарей, в которых используется оцинкованный (горячеоцинкованный или предварительно оцинкованный) Unistrut. Панели солнечных батарей анодированы (обычно черного цвета). Мы используем нержавеющие болты, чтобы прикрепить панели к unistrut. Болты крепятся через алюминиевые монтажные отверстия, открытые для алюминия. Произойдет ли гальваническая реакция при такой конфигурации? Он устанавливается на плоской коммерческой крыше и полностью открыт для атмосферных воздействий.
Эли Ротшильд, производитель — Сан-Франциско, Калифорния
26 августа 2010 г.
А.Уважаемый Эли Ротшильд,
Ответ: ДА.
Единственный вопросительный знак — это временной промежуток, в котором это произойдет. Я не удивлюсь, если в течение года или нескольких лет связь будет потеряна, но у меня нет практического опыта работы с вашей реальной ситуацией (ами). Предпочтительно Al будет растворяться.
Если у вас есть возможность изолировать RVS от алюминия, например использование тефлонового уплотнения уже значительно снизит вероятность возникновения разрушительной гальванической пары.
Если бы вы могли использовать крепеж из одного и того же материала, это было бы даже лучшим решением, хотя все равно будет возникать разность потенциалов из-за того, что две поверхности никогда не равны, и из-за щелевой коррозии.
С уважением,
Гарри ван дер Занден
— Будапешт, Венгрия
A. Привет. Я согласен с Гарри, но лишь частично …
Для возникновения гальванической коррозии необходима токопроводящая жидкость, и я слышал несколько историй о том, что когда единственная жидкость, которой подвергается соединение, — это дождевая вода, это действительно не проблема.Конечно, это может быть смягчено тем, находится ли место установки рядом с морем или промышленность, которая может вызвать сильные кислотные дожди.
Если бы отверстия были предварительно просверлены и анодированы, а не были бы голыми, как вы упомянули, я думаю, проблема была бы очень незначительной. Ввиду оголенного алюминия в отверстиях я считаю, что следует использовать изолирующие втулки и шайбы.
С уважением,
Тед Муни, P.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
12 июля 2012
В.Может ли кто-нибудь помочь мне с этой проблемой: кровле всего около 18 месяцев, и уже появляются черные пятна ржавчины (от 1/2 до 3 дюймов в диаметре) в разных местах, вся кровля под солнечными батареями капает линии также имеют сильную белую ржавчину или окисление?
Джесси Виллеттс— Дейнтри, QLD, АВСТРАЛИЯ
25 июня 2014 г. — эта запись добавлена к этой теме редактором вместо создания дублирующейся темы
В. Мы монтируем солнечные панели различных типов (обычно с анодированным алюминиевым каркасом) на стандартном, готовом к продаже оцинкованном канале Unistrut.Это позволяет производить очень рентабельные и надежные конструкции.
Недавно мое внимание привлекла проблема смешения материалов. Я никогда не видел никаких проблем в этой области, но наши самые старые установки эксплуатируются всего 10 лет.
Есть какие-нибудь мудрые слова по этому поводу?
Спасибо
Маркус Маэдл, установщик солнечных батарей— Сан-Диего, Калифорния, США
31 марта 2012 г.
В. Я начинаю производить изделие из мягкой стали с цинковым, никелевым или порошковым покрытием.Будет ли никелевое или цинковое покрытие достаточно прочным, чтобы противостоять коррозии, когда его кладут на алюминиевую опору? Мы склоняемся к никелю. Будет ли коррозия сохраняться, но в течение более длительного периода времени? Другая причина, по которой мы склоняемся к никелю, заключается в том, что он подвержен воздействию дорожной соли в некоторых частях страны. Спасибо
Брюс РобинсонНовый производитель — Регина Саскачеван, Канада
4 апреля 2012 г.
А. Привет, Брюс.
Когда разнородные материалы соприкасаются друг с другом, возникает вопрос не только выбора антикоррозийных покрытий, но и покрытий, гальванически совместимых друг с другом.По этой причине цинк, вероятно, будет лучше никеля при контакте с алюминием, поскольку они достаточно близко друг к другу в гальванической серии.
Тонкого цинкования будет недостаточно. Я бы предложил либо цинкование плюс порошковое покрытие (которое может уменьшить или устранить гальваническую коррозию), либо горячее цинкование (то есть толстое покрытие цинка).
С уважением,
Тед Муни, P.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
Гвозди оцинкованные с цинковой кровлей
5 августа 2012 г.В.У меня есть кровельные листы из цинковых квасцов. У нас есть стальные оцинкованные гвозди для крепления листов к стропилам. Это скоро вызовет проблемы? Что за беда? Не лучше ли попробовать купить гвозди из квасцов цинка или другого металла?
Мэрилин Штейн— Ваиево, Тавеуни, Фиджи
июнь 2014
A. Привет, Мэрилин. У меня нет личного опыта в этом, но я слышал, что панели из цинковых квасцов довольно хорошо «устраняют» любые гальванические проблемы с гальваническими материалами.
С уважением,
Тед Муни, П.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
4 сентября 2012
Q. Мой вопрос относительно проекта я сейчас делаю, я хотел бы закрепить CORTEN стали на алюминиевой раме, сталь будет облицовка для моей двери гаража и алюминия опорная рама держит обшивку. Поскольку Corten — это естественно корродирующая сталь, будет ли проблема закрепить это на алюминии или есть проблема с болтами, если да, следует ли мне использовать нержавеющие или оцинкованные болты для смягчения этого?
Поскольку Corten — это естественно корродирующая сталь, будет ли проблема закрепить это на алюминии или есть проблема с болтами, если да, следует ли мне использовать нержавеющие или оцинкованные болты для смягчения этого?
— Мельбурн, Виктория, Австралия
12 ноября 2012 г.
А.Здравствуйте, мистер Латимер,
. Прошло 2 месяца с тех пор, как вы разместили свой вопрос, и я очень надеюсь, что вы использовали болты из нержавеющей стали, а не с цинковым покрытием, так как цинк может как-то испортить спорт. SS больше похожа на Corten Steel с точки зрения легирующих элементов, а цинк может вызвать проблемы.
Khozem Vahaanwala
Saify Ind
Bengaluru, Karnataka, India
июнь 2014
А. Привет. Я думаю, что в этом случае я бы хотел использовать винты / болты из стекловолокна или изоляторы на металлических болтах.
С уважением,
Тед Муни, P.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
25 декабря 2012
В. Привет, возникнут ли проблемы с коррозией при использовании стрингеров из горячеоцинкованной стали с алюминиевыми ступенями, прикрученными болтами? Какие болты лучше всего использовать?
Привет, возникнут ли проблемы с коррозией при использовании стрингеров из горячеоцинкованной стали с алюминиевыми ступенями, прикрученными болтами? Какие болты лучше всего использовать?
— Монтвилл, Квинсленд, Австралия
28 декабря 2012 г.
A. Болты, оцинкованные горячим способом, подойдут в вашем случае.
Khozem Vahaanwala
Saify Ind
Bengaluru, Karnataka, India
(вы на 1-й странице) Следующая страница>
нареч.
этот текст заменяется на bannerText
Заявление об ограничении ответственности: с помощью этих страниц невозможно полностью диагностировать проблему отделки или опасности операции. Вся представленная информация предназначена для общего ознакомления и не отражает профессионального мнения или политики работодателя автора. Интернет в основном анонимный и непроверенный; некоторые имена могут быть вымышленными, а некоторые рекомендации могут быть вредными.
Если вы ищете продукт или услугу, связанную с отделкой металлов, пожалуйста, посетите эти каталоги:
О нас / Контакты — Политика конфиденциальности — © 1995-2021 finish.com, Pine Beach, New Jersey, USA
Какие материалы крепежа работают с алюминием, не вызывая его коррозии?
Алюминий — легкий, гибкий и прочный металл, поэтому неудивительно, что он так широко используется во всем, от аэронавтики до медицинского оборудования. Однако алюминий затрудняет выбор крепежа для вашего проекта, потому что он очень склонен к реакции с другими металлическими веществами и коррозии.
Коррозия может стать препятствием, когда вы планируете контейнер под давлением или самолет, который будет перевозить пассажиров высоко в небо.Небольшая коррозия в этих случаях приводит к серьезным последствиям. Благодаря широкому выбору материалов для крепежа, доступных сегодня, нужно просто выбрать один из следующих вариантов, которые не будут подвержены коррозии при контакте с алюминием.
Сталь с покрытием
При достаточно толстом покрытии даже очень реактивный металл, такой как латунь, можно использовать на алюминиевой конструкции без коррозии. Поскольку нержавеющая сталь остается одним из наименее реактивных металлов без покрытия, разумнее использовать ее в качестве основного материала.Если какое-либо покрытие отсутствует, оголенный металл по-прежнему вызывает меньше коррозии и вызывает меньше катастрофических отказов.
Есть много способов покрытия стальных крепежных изделий, но большинство из них включает связующее, смешанное с хлопьями некоррозионного элемента, такого как цинк. Для непосредственного использования алюминия существует возможность покрытия крепежных деталей смесью, в которую входят, в частности, алюминиевые чешуйки. Это покрытие делает практически любой крепеж безопасным для использования с алюминием, пока покрытие остается неповрежденным.
Хорошей идеей будет покрасить крепежные детали перед установкой, чтобы создать дополнительный слой, который может блокировать коррозию, но краска недостаточно прочная, чтобы полагаться на нее как на единственное покрытие. Краска соскабливается во время установки, поэтому используйте ее только как запасной вариант для добавления дополнительного уровня защиты.
Краска соскабливается во время установки, поэтому используйте ее только как запасной вариант для добавления дополнительного уровня защиты.
Сталь с гальваническим покрытием
Один из старейших способов нанесения покрытия на сталь — это процесс, известный как гальванизация. Это форма гальваники, которая включает нанесение слоя коррозионно-стойкого металла на внешнюю часть застежки или другого компонента.
Поскольку гальваника или гальваника включает электричество, она создает очень плотную связь между поверхностью металла и защитным покрытием. Однако покрытие может стираться с возрастом или царапаться во время укладки. Именно поэтому многие производители перешли на другие покрытия, обладающие большей стойкостью.
Гальваника остается более распространенной, чем высокотехнологичные покрытия, которые были разработаны совсем недавно. Если стоимость является проблемой, оцинкованные крепежные детали, как правило, дешевле, чем с покрытием, но при этом обладают почти такой же устойчивостью к коррозии.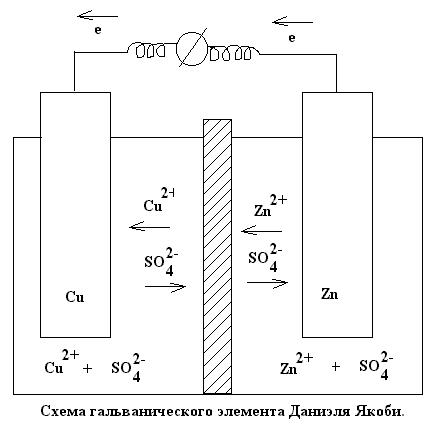
Алюминий
Один из типов коррозии известен как реакция двух металлов. Присутствие влаги обеспечивает электрическое соединение между двумя разными металлами, вызывая обмен, который делает один из них слабым и ямочным. Использование одного и того же металла для всех частей вашего проекта полностью устраняет эту проблему. Поскольку покрытия нет, царапины тоже не приводят к коррозии.
Тем не менее, алюминий — не всегда лучший крепежный материал.Он не обладает такой же прочностью, когда дело доходит до сопротивления сдвигу, и это часто является определяющим фактором при выборе крепежа для такого проекта, как самолет или пригородный поезд. Алюминиевые крепежи обычно используются в менее тяжелых условиях.
Неметаллические крепежные детали
Наконец, крепежные детали из различных высокопрочных пластмасс, доступных сегодня, также являются вариантом предотвращения коррозии алюминия. Неметаллические болты и винты даже более ограничены по прочности, чем алюминиевые, но они по-прежнему являются хорошим вариантом для медицинских и пищевых производств.
Для большинства применений крепеж из стали с покрытием или оцинковки — лучший вариант для соединения с алюминием. Но варианты на этом не заканчиваются. Не уверены, какая марка или тип стали вам нужна? Сообщите нам подробности вашего проекта здесь, в Ascension Fasteners. , И мы поможем вам сделать правильный выбор.
FAQ 1: Гальваническая коррозия / коррозия разнородных металлов
Контакт между разнородными металлами происходит часто, но часто не является проблемой. Алюминиевая головка на чугунном блоке, припой на медной трубе, гальваника на стальной обрешетке и стальной крепеж в алюминиевом листе — типичные примеры.
Скачать FAQ по ASSDA 1 (PDF)
ЧТО ВЫЗЫВАЕТ ГАЛЬВАНИЧЕСКУЮ КОРРОЗИЮ?
Для возникновения гальванической, разнородной или электролитической коррозии должны быть выполнены три условия:
- Металлическое соединение должно быть смочено токопроводящей жидкостью
- Должен быть контакт металл к металлу
- Металлы должны иметь достаточно разные потенциалы
Смачивание стыка
Проводящей жидкостью (или электролитом) может быть дождевая вода или вода, абсорбированная поверхностными отложениями, если относительная влажность (RH) достаточно высока, или даже простая конденсация. Если отложения представляют собой морскую соль, они начнут растворяться, если относительная влажность превысит 34% из-за хлорида магния. Чем выше проводимость, тем сильнее гальванические эффекты. Соляное или промышленное загрязнение значительно увеличивает проводимость воды, поэтому гальванические эффекты обычно более сильны у побережья или в тяжелых промышленных зонах. Чистая дождевая вода с низкой проводимостью вызовет лишь незначительные гальванические эффекты. Одна из сложностей заключается в том, что во время испарения водяные пленки становятся более проводящими, поэтому изначально чистая вода может вызывать довольно активные гальванические эффекты, поскольку жидкость в щели под болтом или зажимом становится более концентрированной.Вода может быть исключена за счет конструкции или использования адгезивных герметиков или окраски благородного металла на 30–50 мм за стыком, чтобы предотвратить перенос заряженных атомов (ионов) в любой тонкой водной пленке. Покраска активного металла (углеродистой стали, алюминия или цинка) может вызвать глубокие отверстия на дефектах покрытия.
Если отложения представляют собой морскую соль, они начнут растворяться, если относительная влажность превысит 34% из-за хлорида магния. Чем выше проводимость, тем сильнее гальванические эффекты. Соляное или промышленное загрязнение значительно увеличивает проводимость воды, поэтому гальванические эффекты обычно более сильны у побережья или в тяжелых промышленных зонах. Чистая дождевая вода с низкой проводимостью вызовет лишь незначительные гальванические эффекты. Одна из сложностей заключается в том, что во время испарения водяные пленки становятся более проводящими, поэтому изначально чистая вода может вызывать довольно активные гальванические эффекты, поскольку жидкость в щели под болтом или зажимом становится более концентрированной.Вода может быть исключена за счет конструкции или использования адгезивных герметиков или окраски благородного металла на 30–50 мм за стыком, чтобы предотвратить перенос заряженных атомов (ионов) в любой тонкой водной пленке. Покраска активного металла (углеродистой стали, алюминия или цинка) может вызвать глубокие отверстия на дефектах покрытия.
Контакт металл-металл
Гальваническая коррозия может возникнуть только в том случае, если разнородные металлы находятся в электрическом контакте. Контакт может быть прямым или посредством внешней трубы, провода или болта.Если разнородные металлы изолированы друг от друга подходящими пластиковыми полосами, шайбами или втулками, то гальваническая коррозия не может возникнуть. Краска не является надежным электрическим изолятором, особенно под головками болтов, гайками, шайбами или возле краев металлических листов. Краска обычно повреждается при установке или последующем перемещении. Обратите внимание, что слой пленки оксида хрома на нержавеющей стали очень тонкий и не является электрическим изолятором. Поэтому пленка оксида хрома не предотвращает гальваническую коррозию.
Различия потенциалов
Все металлы в некоторой степени растворяются при смачивании токопроводящей жидкостью. Степень растворения наиболее высока для активных или жертвенных металлов, таких как магний и цинк, и они имеют самый отрицательный потенциал.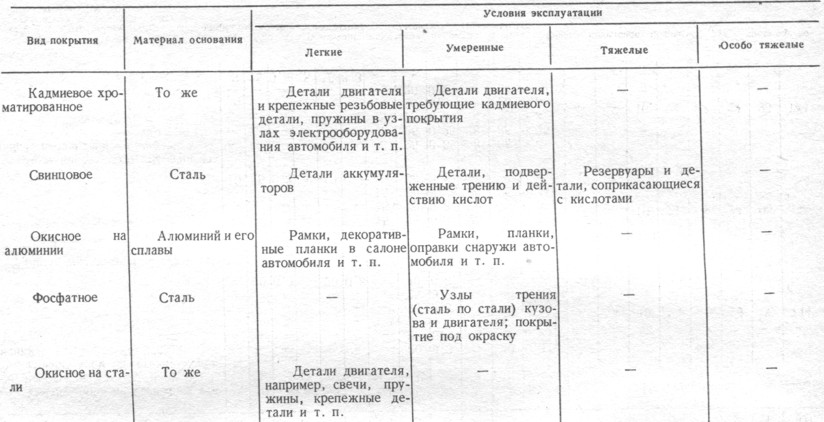 Напротив, благородные или пассивные металлы, такие как золото или графит, относительно инертны и имеют более положительный потенциал. Посередине находится нержавеющая сталь, хотя она более благородна, чем углеродистая сталь. Потенциал можно измерить с помощью электрода сравнения и использовать для построения гальванической серии, как показано ниже (стандарт ASTM G82).
Напротив, благородные или пассивные металлы, такие как золото или графит, относительно инертны и имеют более положительный потенциал. Посередине находится нержавеющая сталь, хотя она более благородна, чем углеродистая сталь. Потенциал можно измерить с помощью электрода сравнения и использовать для построения гальванической серии, как показано ниже (стандарт ASTM G82).
Когда два металла соединяются и контактируют с проводящей жидкостью, более активный металл вызывает коррозию и защищает благородный металл. Цинк более негативен, чем сталь, поэтому цинковое покрытие оцинкованной стали подвержено коррозии, чтобы защитить сталь от царапин или порезов. Нержавеющие стали, в том числе 304 и 316, более положительны, чем цинк и сталь, поэтому, когда нержавеющая сталь соприкасается с оцинкованной сталью и является влажной, сначала коррозирует цинк, затем сталь, а нержавеющая сталь будет защищена эта гальваническая активность и не вызывает коррозии.Скорость гальванической атаки определяется величиной разности потенциалов.
График показывает, что нержавеющая сталь имеет два диапазона потенциала. Обычное пассивное поведение показано светлой штриховкой. Однако, если пассивная пленка разрушается, нержавеющая сталь подвергается коррозии, и ее потенциал находится в диапазоне темных полос.
Как показывает опыт, если разность потенциалов меньше 0,1 В, то гальваническая коррозия маловероятна.
Если все три условия соблюдены, то вероятна гальваническая коррозия, и на скорость коррозии будут влиять относительная площадь и плотность тока, подаваемого благородным металлом.
ОТНОСИТЕЛЬНАЯ ПОВЕРХНОСТЬ, СМАЧИВАЕМАЯ СМАЗКОЙ
Если благородный металл, такой как нержавеющая сталь, имеет большую площадь поверхности, контактирующую с электролитом, а жертвенный металл (например, алюминий) имеет очень маленькую площадь поверхности, контактирующую с электролитом, то нержавеющая сталь будет генерировать большой ток коррозии, который будет сосредоточено на небольшой площади жертвенного металла. Алюминий быстро подвергается коррозии, поэтому алюминиевые крепежи из нержавеющей стали неприемлемы.Однако часто используется нержавеющий винт из алюминия, хотя коррозия алюминия непосредственно вокруг нержавеющей стали вполне возможна. Это связано с тем, что соотношение смоченной благородной застежки A в активном металле может измениться с 1:50 до 1: 1 во время высыхания после ливня. Если загрязняющие вещества значительны, это означает, что избегание пар разнородных металлов может быть предпочтительным вариантом для предотвращения гальванической атаки.
Алюминий быстро подвергается коррозии, поэтому алюминиевые крепежи из нержавеющей стали неприемлемы.Однако часто используется нержавеющий винт из алюминия, хотя коррозия алюминия непосредственно вокруг нержавеющей стали вполне возможна. Это связано с тем, что соотношение смоченной благородной застежки A в активном металле может измениться с 1:50 до 1: 1 во время высыхания после ливня. Если загрязняющие вещества значительны, это означает, что избегание пар разнородных металлов может быть предпочтительным вариантом для предотвращения гальванической атаки.
Гальванизированные крепежные детали из нержавеющей стали также теряют цинк быстрее, чем отдельные изделия.Дополнительным недостатком является то, что продукт коррозии изменит цвет с белого на оранжевый, когда коррозия достигнет сплава цинка с железом около нижней части гальванизированного слоя. После этого начинается коррозия крепежа из углеродистой стали — снова более быстрыми темпами, чем при автономном воздействии.
Как показывает опыт, если смачиваемая площадь корродирующего металла в 10 раз больше смачиваемой площади благородного металла, то гальванические эффекты не являются серьезными, хотя чем больше это отношение, тем меньше эффект.
ДОСТУПНАЯ ПЛОТНОСТЬ ТОКА Нержавеющая сталь
имеет эффективную пассивную пленку, поэтому доступный ток коррозии, переносимый заряженными атомами (ионами), довольно низок.Если сравнивать поведение пары медь / сталь и пары нержавеющая сталь / сталь, муфта медь / сталь представляет собой более серьезную гальваническую проблему, несмотря на аналогичное разделение потенциалов в 0,35 В.
Примеры приемлемых гальванических пар:
- Потенциал медного сплава более активен, чем у нержавеющей стали, и он обеспечивает ток катодной защиты для ограничения точечной коррозии вала из нержавеющей стали или проникновения трещин на втулку подшипника. Глубина потери медного сплава невелика, поскольку он имеет очень большую площадь по сравнению с обнаженным валом.
- Подвески для труб из оцинкованной стали используются для внешней подвески труб из нержавеющей стали вокруг химических заводов. Отношение площади поверхности плохое при большой площади нержавеющей стали и небольшой площади активного цинка / стали, но дождевая вода обычно имеет довольно низкую проводимость, и 20-летний срок службы является нормальным.

- В водной промышленности заедание между резьбой из нержавеющей стали и гайками удалось избежать за счет использования гайки из алюминиевой бронзы на шпильках или болтах из нержавеющей стали. Хотя алюминиевая бронза более активна, чем нержавеющая сталь, проводимость воды и, следовательно, скорость коррозии, как правило, довольно низкая.Гайки потребуют замены, но только во время капитального ремонта.
- Разница потенциалов между пассивным элементом 304 и пассивным элементом 316 невелика, поэтому гальваническая коррозия 304 не ожидается даже при больших соотношениях площадей.
Неприемлемые пары материалов включают резиновое уплотнение с настолько высоким содержанием технического углерода (для устойчивости к ультрафиолетовому излучению), что оно является проводящим и вызывает гальваническое воздействие на винт или штифт из нержавеющей стали. Прокладки, содержащие графит, вызывают аналогичные проблемы для фланцев из нержавеющей стали, и их нельзя использовать для морской воды независимо от сплава нержавеющей стали. Неизолированные крепления из нержавеющей стали не допускаются для настенного или кровельного покрытия Colorbond®, так как гальванический ток от корродирующего Zincalume® вызывает вздутие краски.
Неизолированные крепления из нержавеющей стали не допускаются для настенного или кровельного покрытия Colorbond®, так как гальванический ток от корродирующего Zincalume® вызывает вздутие краски.
СЕРИЯ GALVANIC
ВАЖНЫЙ ОТКАЗ ОТ ОТВЕТСТВЕННОСТИ: Технические рекомендации, содержащиеся в этой публикации, обязательно носят общий характер, и на них нельзя полагаться для конкретных приложений без предварительного получения компетентного совета. Несмотря на то, что ASSDA предприняла все разумные шаги для обеспечения точности и актуальности информации, содержащейся в данном документе, ASSDA не гарантирует точность или полноту информации и не несет ответственности за ошибки или упущения.
Нержавеющая сталь и алюминий: почему не следует использовать их вместе и соответствующие меры предосторожности, если вы это сделаете
Гальваническая коррозия
Комбинация алюминия и нержавеющей стали вызывает гальваническую коррозию. Чтобы понять, почему не следует использовать вместе нержавеющую сталь и алюминий, нам сначала нужно понять, как работает гальваническая коррозия. Гальваническая коррозия — это перенос электронов от одного материала (анода) к другому (катоду). Помимо знания того, что такое гальваническая коррозия, нам также необходимо понимать связанные с ней технические термины.
Чтобы понять, почему не следует использовать вместе нержавеющую сталь и алюминий, нам сначала нужно понять, как работает гальваническая коррозия. Гальваническая коррозия — это перенос электронов от одного материала (анода) к другому (катоду). Помимо знания того, что такое гальваническая коррозия, нам также необходимо понимать связанные с ней технические термины.
Вот все технические термины, которые мы будем использовать в этой публикации:
- Анод — материал, который заряжен положительно, электроны покидают этот материал
- Катод — материал, который заряжен отрицательно, в этот материал входят электроны
- Электролит — жидкость, помогающая в процессе переноса электронов
- Коррозия / коррозия — постепенное разрушение или ослабление металла
Как это работает
Гальваническая коррозия возникает, когда два материала (анод и катод) контактируют друг с другом и с электролитом.Электролиты могут быть факторами окружающей среды, такими как влажность или дождевая вода.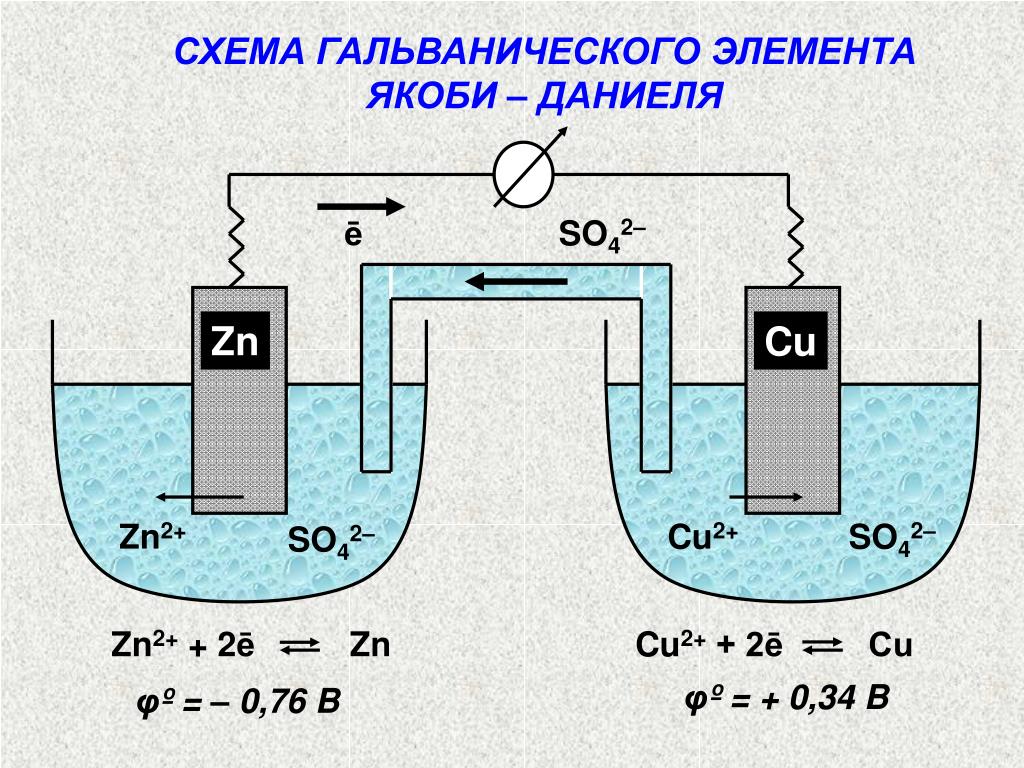 Когда эти факторы вступят в силу, начнется перенос электронов. В зависимости от уровня сопротивления электролита этот перенос может происходить намного быстрее. Вот почему соленая вода, электролит с очень низким сопротивлением, является общим фактором при выборе продукта. В связи с этим невероятно важно продумать, какой материал вы собираетесь использовать в окружающей среде. При работе с морской или соленой водой вам даже нужно учитывать тип нержавеющей стали, которую вы используете.
Когда эти факторы вступят в силу, начнется перенос электронов. В зависимости от уровня сопротивления электролита этот перенос может происходить намного быстрее. Вот почему соленая вода, электролит с очень низким сопротивлением, является общим фактором при выборе продукта. В связи с этим невероятно важно продумать, какой материал вы собираетесь использовать в окружающей среде. При работе с морской или соленой водой вам даже нужно учитывать тип нержавеющей стали, которую вы используете.
Существует несколько видов ржавчины, которые могут возникнуть в процессе окисления. Чтобы узнать о них больше, прочтите это сообщение в блоге о трех часто встречающихся типах ржавчины.
Наш пример
В оставшейся части нашего сообщения, вместо того, чтобы ссылаться на анод и катод, мы будем использовать пример алюминия (анод) и нержавеющей стали (катод). Когда алюминий и нержавеющая сталь используются в сборке вместе, электроны из алюминия начнут переходить в нержавеющую сталь. Это приводит к ослаблению алюминия. Этот ослабленный алюминий заставляет его ухудшаться гораздо быстрее. Это может продлить срок службы нержавеющей стали. Примечание: Алюминий, если оставить его вместе с электролитом, со временем все равно будет терять свои электроны, но наличие нержавеющей стали значительно ускорит этот процесс.
Это приводит к ослаблению алюминия. Этот ослабленный алюминий заставляет его ухудшаться гораздо быстрее. Это может продлить срок службы нержавеющей стали. Примечание: Алюминий, если оставить его вместе с электролитом, со временем все равно будет терять свои электроны, но наличие нержавеющей стали значительно ускорит этот процесс.
Практика гальванической коррозии обычно используется при нанесении покрытия для создания временного слоя поверх другого материала. Обычно используются оцинкованная сталь и черный оксид.
Исключения
Каждая сборка ситуативна. Поскольку металл подвержен коррозии за счет факторов окружающей среды, могут быть места, где вы можете использовать некоторые металлы вместе, не заметив этих эффектов. Если окружающая среда очень сухая, защищенная от непогоды и грязи, вы можете попробовать использовать металлы вместе. Однако в большинстве случаев окружающая среда не контролируется температурой и влажностью, возникает ржавчина. По этой причине компания Albany County Fasteners рекомендует никогда не использовать вместе алюминий и нержавеющую сталь. Мы также рекомендуем использовать исключительно металлы для максимального срока службы. Нержавеющая сталь с нержавеющей, алюминий с алюминием, латунь с латунью. Смешивание металлов может повлиять на прочность покрытия, срок службы крепежа, коррозию материалов и т. Д.
Мы также рекомендуем использовать исключительно металлы для максимального срока службы. Нержавеющая сталь с нержавеющей, алюминий с алюминием, латунь с латунью. Смешивание металлов может повлиять на прочность покрытия, срок службы крепежа, коррозию материалов и т. Д.
Другая ситуация, в которой эти материалы могут использоваться вместе с небольшим воздействием на предотвращение ржавчины, — это если площадь катода очень мала по сравнению с площадью анода. Например, если основным материалом является большой лист алюминия, то использование очень маленьких винтов из нержавеющей стали не приведет к значительному сокращению срока службы.И наоборот, если вы используете алюминий для крепления большого листа нержавеющей стали, срок службы алюминия резко сократится.
Albany County Fasteners рекомендует использовать неопрен EPDM или связующие шайбы между нержавеющими крепежными деталями и алюминиевыми материалами, неопрен образует барьер между металлами, предотвращая коррозию.
Факторы окружающей среды для определения
При выборе материала, подходящего для вашей установки, необходимо учитывать множество факторов.
| Фактор | Почему это важно |
| Продолжительность контакта с электролитом | Чем дольше электролит находится в контакте с алюминием и нержавеющей сталью, тем выше вероятность переноса электронов. |
| Электролитное сопротивление | Чем ниже сопротивление электролита, тем легче происходит перенос электронов. Пример: соленая вода имеет очень низкое сопротивление электролиту. |
| Стоячая вода | Вода, которая сидит и рассеивается очень долго, может привести к продолжительному воздействию электролитов. |
| Грязь | Грязь (особенно не под прямыми солнечными лучами) может абсорбировать электролит и удерживать его в течение очень долгого времени. Это может привести к увеличению контакта с узлом, если его не поддерживать в чистоте. Это может привести к увеличению контакта с узлом, если его не поддерживать в чистоте. |
| Влажность / туман | Оба фактора окружающей среды приводят к увеличению содержания воды в воздухе.Если окружающая среда подвержена этим факторам, воздействие электролитов считается увеличенным |
| Щели | Щели служат для улавливания влаги (электролита), которая может удерживать ее на материалах в течение длительного периода времени. |
Благородные металлы
Если вы решите, что вам нужно использовать два разных материала вместе, мы рекомендуем использовать анод в качестве основного материала и убедиться, что он значительно больше катодов.Катоды также можно назвать благородными металлами или металлами, обладающими высокой стойкостью к окислению (ржавчине). Ниже мы составили список благородных металлов:
- Золото
- Иридий
- Меркурий
- Осмий
- Палладий
- Платина
- Родий
- Рутений
- Серебро
От анода к катоду
Чтобы еще больше снизить влияние гальванической коррозии, рекомендуется использовать материалы, которые с меньшей вероятностью вызывают перенос электронов при контакте друг с другом и электролитом. Следующий список представляет собой список материалов. * Примечание: чем ближе два металла в этом списке, тем меньше вероятность того, что они пострадают от отрицательного воздействия гальванической коррозии.
Следующий список представляет собой список материалов. * Примечание: чем ближе два металла в этом списке, тем меньше вероятность того, что они пострадают от отрицательного воздействия гальванической коррозии.
- Магний
- Магниевые сплавы
- Цинк
- Бериллий
- Алюминиевые сплавы
- Кадмий
- Низкоуглеродистая и углеродистая сталь, чугун
- Хромистая сталь (с содержанием хрома менее или равного 6%)
- Активная нержавеющая сталь (302, 310, 316, 410, 430)
- Алюминиевая бронза
- Свинцово-оловянный припой
- Олово
- Активный никель
- Активный инконель
- Латунь
- бронза
- Медь
- Марганцевая бронза
- Силиконовая бронза
- Медно-никелевые сплавы
- Свинец
- Монель
- Серебряный припой
- Пассивный никель
- Пассивный инконель
- Пассивная нержавеющая сталь (302, 310, 316, 410, 430)
- Серебро
- Титан
- Цирконий
- Золото
- Платина
Как остановить гальваническую коррозию?
Есть несколько шагов, которые вы можете предпринять, если ДОЛЖНЫ использовать эти материалы вместе.
- Добавьте изолятор между двумя материалами, чтобы они больше не соединялись. Без этой связи передача электронов невозможна. Гайки для колодцев — это обычно используемый крепеж для отделения материалов, которые могут пострадать от гальванической коррозии.
- Используйте материалы с одинаковым потенциалом. Металлы с одинаковой коррозионной стойкостью обычно можно использовать вместе.
- Если вы находитесь в ситуации, когда только один из материалов будет контактировать с электролитом, перенос электронов не произойдет.
- Если на катоде есть покрытие, оно может предотвратить перенос из-за повышенного сопротивления.
- Примите во внимание вашу среду перед установкой. Выберите материалы, которые подходят для вашей среды.
- Покройте или покрасьте сборку (полностью), чтобы электролит не контактировал с материалами
- Используйте неопрен EPDM или связующие шайбы в качестве барьера между металлами.
Если вам интересны типы материалов, которые мы предлагаем, и дополнительная информация о них, ознакомьтесь с нашим Справочным руководством по материалам.
Совместимость алюминия и стали
МАТЕРИАЛЫ, ТАКИЕ КАК , бетон, металлы, полимеры и древесина, используемые в строительной отрасли, часто смешиваются для обеспечения желаемых эстетических, структурных и погодостойких функций.
Смешивание материалов имеет значение
Иногда такая конструкция из смешанных материалов может привести к проблемам совместимости, таким как окрашивание поверхностей или ускоренное разрушение, особенно в сильно коррозионных средах.
Одним из примеров является ускоренная коррозия гвоздей, оцинкованных горячим способом, при забивании влажной древесины, обработанной определенными медьсодержащими консервантами.
Другой случай, когда два разнородных материала, не находящихся в прямом контакте друг с другом, подвергаются стеканию воды, например, воде, текущей с предварительно окрашенной стальной поверхности, что может вызвать преждевременный выход из строя оцинкованной стали, установленной под ней (рис.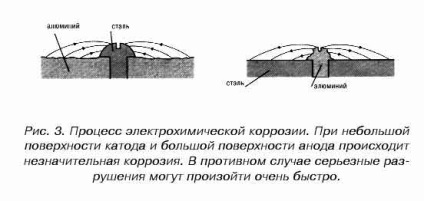 1).
1).
Проблемы, связанные с соединением алюминия и нержавеющей стали.
Алюминий и нержавеющая сталь — это сочетание материалов, которое часто привлекает внимание и уже давно используется там, где длительный срок службы важен для целостности и производительности зданий.
В определенных обстоятельствах, в зависимости от конструкции или установки, это может привести к высокому риску коррозии и, следовательно, к преждевременному выходу из строя алюминиевых компонентов. В других случаях значительной коррозии не наблюдалось.
Что происходит и почему?
Наука, лежащая в основе этого, — гальваническая коррозия. Это процесс, вызванный разностью электрохимических потенциалов между двумя разнородными металлами, которые электрически связаны с наличием электролита — например, слоя воды.
Алюминий активен и имеет электрохимический потенциал от -0,76 до -0,99 В в морской воде.
Нержавеющая сталь, например, марки 304, наиболее широко используемая нержавеющая сталь в зданиях Новой Зеландии, имеет более положительный потенциал, чем алюминий.Когда на его поверхности образуется пассивная тонкая оксидная пленка с высоким содержанием хрома, марка 304 имеет потенциал в диапазоне от -0,05 до -0,13 В. Когда эта пленка разрушается, потенциал находится в диапазоне от -0,45 до -0,57 В.
Когда эти два При контакте материалов разность потенциалов превышает 0,2 В. Следовательно, это может привести к образованию ячеек гальванической коррозии и риску коррозии алюминия.
Вернуться к началу
Другие факторы также имеют значение
Гальваническая коррозия может быть серьезной в условиях полного погружения.В атмосферных условиях это произойдет, когда контактная площадка будет достаточно влажной в течение длительного периода времени. Они зависят от местных климатических условий, включая количество и частоту дождя, скорость испарения и время увлажнения.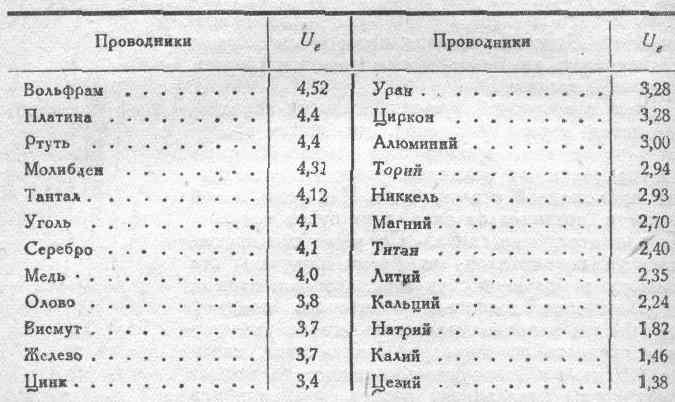
В благоприятных атмосферных условиях конденсация влаги или дождевая вода с ограниченным растворением агрессивных сред могут перекрыть контакт между этими материалами. Однако гальваническая коррозия протекает медленно. В морской среде частицы соли могут осаждаться вокруг контакта, что значительно увеличивает проводимость влаги и слоя воды, что приводит к большему риску коррозии.
Относительные площади поверхностей двух сопряженных металлов чрезвычайно важны для фактического риска гальванической коррозии. В большинстве природных сред этот риск можно значительно снизить, если более активный металл имеет гораздо большую относительную площадь поверхности по сравнению с менее активным металлом.
Расстояние тоже играет свою роль. Гальваническая коррозия в атмосферных условиях обычно локализуется вокруг точки контакта. Он будет уменьшаться по мере удаления от области контакта.
Где и то и другое можно безопасно использовать
Алюминий и нержавеющая сталь можно безопасно использовать вместе в зонах воздействия B и C, как это определено картой атмосферной коррозии в NZS 3604: 2011 Здания с деревянным каркасом.
В зоне воздействия D, где сильное влияние моря, было бы разумно избегать прямого контакта между этими материалами. Однако, если элемент из нержавеющей стали мал по сравнению с алюминием и подвергается минимальному воздействию морской воды или соленого влажного воздуха, коррозия алюминия будет лишь незначительно увеличиваться. Примером этого является использование болтов, винтов или заклепок из нержавеющей стали в алюминиевых оконных рамах.
Там, где они не могут быть безопасно использованы
Значительно повышенный риск коррозии алюминия из-за его контакта с нержавеющей сталью может иметь место:
- в областях, где влага или дождевая вода могут удерживаться или задерживаться постоянно или в течение длительного периода времени
- в точках сборки кровли или облицовки стен, подверженных воздействию существенно влажной и агрессивной атмосферной среды — например, прибрежных или сильно загрязненных промышленных территорий.
При фиксации анодированных алюминиевых листов или панелей с помощью крепежа из нержавеющей стали тонкий анодированный слой может быть частично поврежден — например, из-за образования небольших трещин.
Небольшая часть алюминиевой подложки будет открыта и может соприкоснуться с нержавеющей сталью (рис. 2). Это может вызвать локальную повышенную гальваническую коррозию алюминия в высококоррозионных средах.
Рис. 2: Контакт между крепежом из нержавеющей стали и частично поврежденным анодированным алюминиевым листом.В очень суровых морских условиях нержавеющая сталь (например, марки 304) все еще может подвергаться коррозии. Слив воды может привести к появлению неприятных пятен или поверхностной коррозии алюминиевых компонентов, установленных ниже (Рисунок 3).
Рис. 3. Пятна на алюминии из-за стекания воды с корродирующей поверхности из нержавеющей стали (марки 304) в суровых морских условиях.Предотвращение гальванической коррозии
Гальваническая коррозия требует одновременного выполнения следующих трех условий:
- Различные типы металлов.
- Наличие электролита в местах контакта.
- Электрическое соединение между двумя металлами.
 Лучший способ предотвратить гальваническую коррозию — избегать использования разнородных металлов. Если это не может быть достигнуто, рассмотрите следующие подходы:
Лучший способ предотвратить гальваническую коррозию — избегать использования разнородных металлов. Если это не может быть достигнуто, рассмотрите следующие подходы: - Конструкция, позволяющая свести к минимуму удержание влаги и воды и осаждение пыли, частиц соли или твердых частиц вокруг области контакта.
- Используйте прочные непроводящие прокладки или шайбы подходящей толщины, чтобы нарушить токопроводящий путь.Полимерная краска на алюминии не всегда может обеспечивать электрическую изоляцию в течение ожидаемого срока службы такой конструкции, поскольку она может разрушаться под воздействием тепла, света или химикатов. Он также может быть механически поврежден другими компонентами, такими как крепежные детали.
- Нанесите прочное полимерное покрытие, чтобы изолировать всю область стыка от окружающей среды. Этот подход популярен в строительстве для изоляции между крепежными элементами и листами кровельной стали.
Доступные руководства
Совместимость материалов следует учитывать на этапах проектирования, строительства и технического обслуживания здания. Общее руководство по совместимости строительных материалов можно найти в:
Общее руководство по совместимости строительных материалов можно найти в:
- E2 / AS1 Таблица 21 Совместимость контактирующих материалов и Таблица 22 Совместимость материалов, подверженных стеканию
- Бюллетень BRANZ 519 Выбор крепежных элементов
- NZ Правила практики металлических кровель и стен v3.0 Таблица 4.10.3C Совместимость материалов .
К началу
Скачать PDF
Чжэнвэй Ли
BRANZ Старший научный сотрудник
Посмотреть все статьи Чжэнвэй Ли
Статьи верны на момент публикации, но с тех пор могут устареть.

 п. (рисунок 12).
п. (рисунок 12).

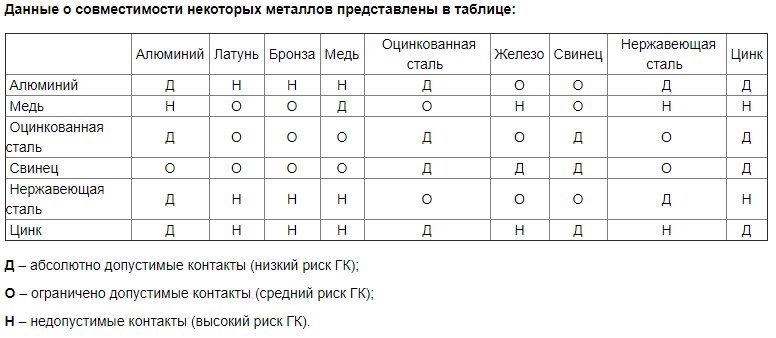 Нередко они образуют весьма сильную гальваническую пару, что приводит к быстрому образованию коррозии в местах их непосредственного соприкосновения.
Нередко они образуют весьма сильную гальваническую пару, что приводит к быстрому образованию коррозии в местах их непосредственного соприкосновения.
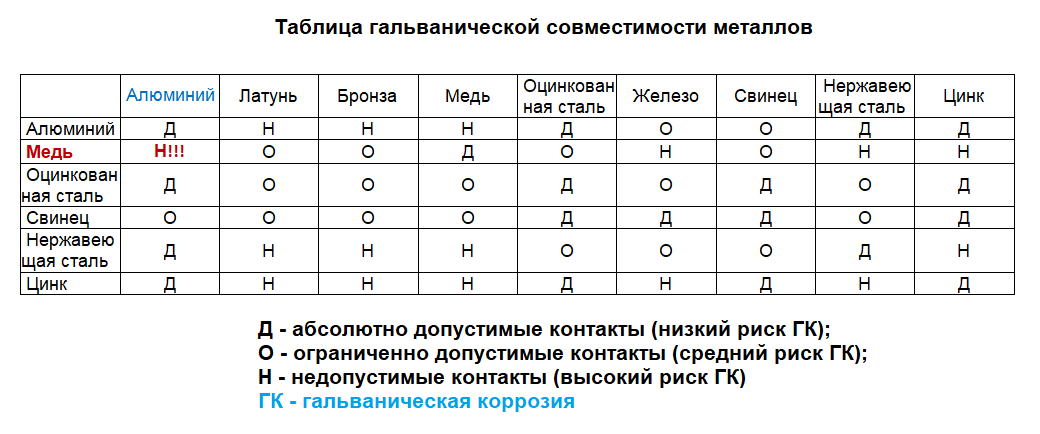
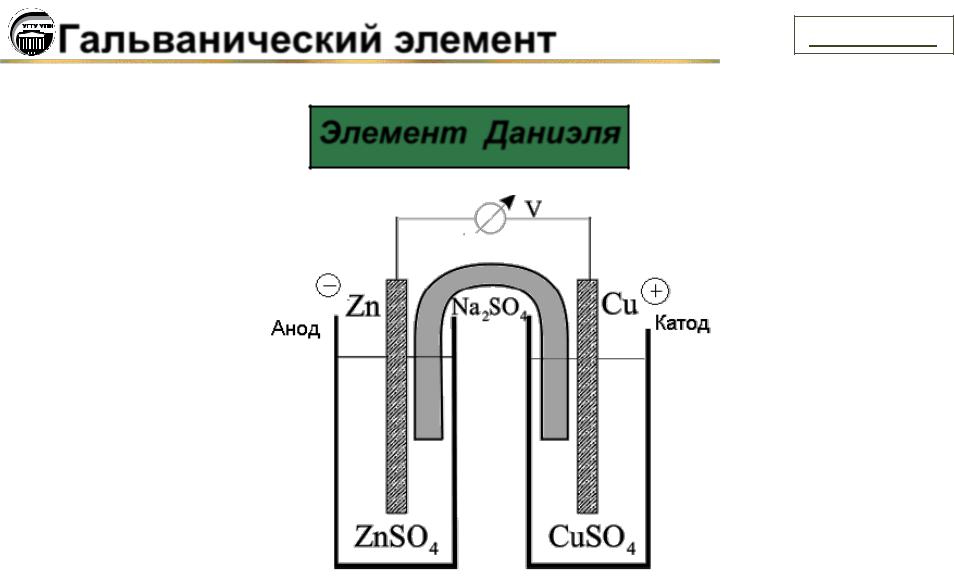
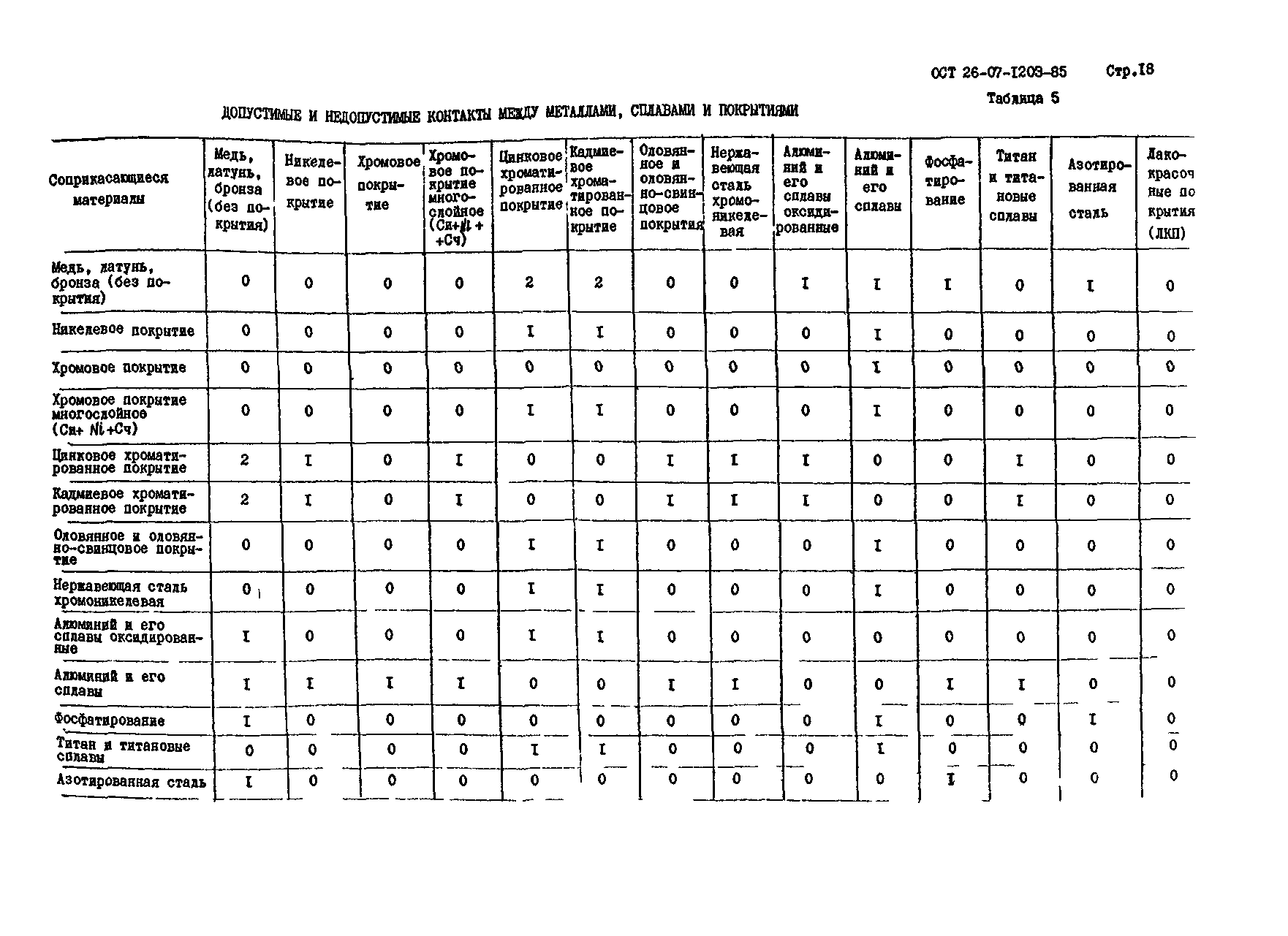
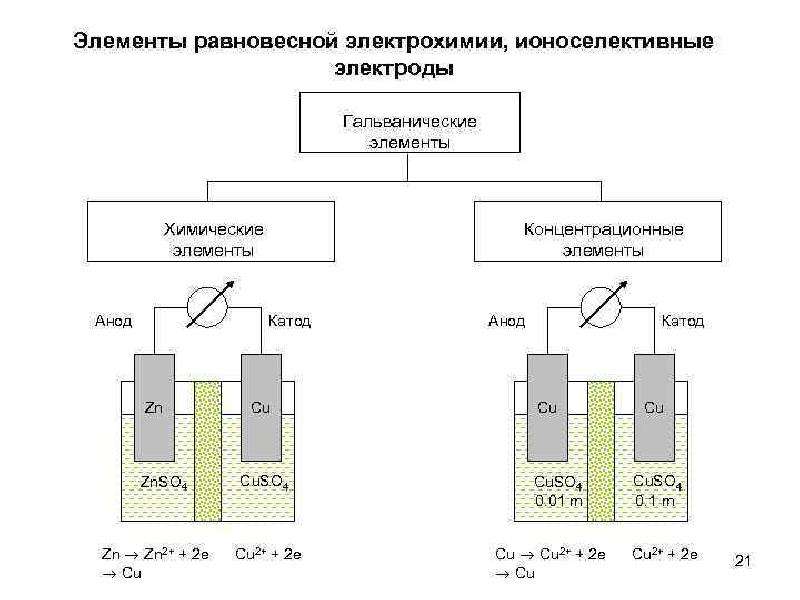
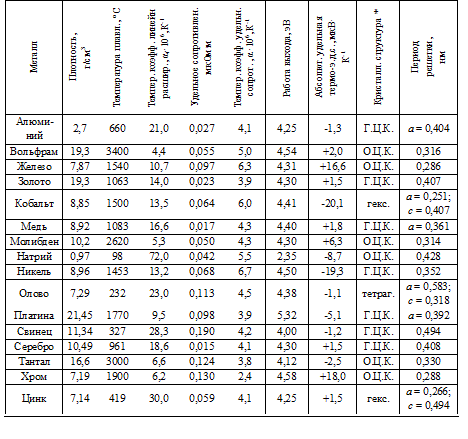 Лучший способ предотвратить гальваническую коррозию — избегать использования разнородных металлов. Если это не может быть достигнуто, рассмотрите следующие подходы:
Лучший способ предотвратить гальваническую коррозию — избегать использования разнородных металлов. Если это не может быть достигнуто, рассмотрите следующие подходы: