Свинцово-кислотный аккумулятор — Википедия
Схема свинцово-кислотного аккумулятора при зарядке (слева) и при подключении потребителя электрического тока Схема расположения электродов в свинцово-кислотном аккумуляторе, пластины катода и анода располагаются попеременно с прослойкой изолятора и объединяется каждый токонесущей полоской в выводы аккумулятора Строение свинцово-кислотного аккумулятора: слева — пластины положительного электрода, изолятора из стекловаты, отрицательного электрода; справа — аккумулятор в сборе (извлечён из корпуса с электролитом). Пластины электродов представляют собой свинцовую (чаще сплав свинца и сурьмы для повышения механической прочности[1]) решётку, ячейки которой заполнены сульфатом свинца со связующим материалом, токонесущие полосы и выводы аккумулятора изготовлены из свинца Варианты электрода свинцово-кислотного аккумулятора Свинцово-кислотный аккумулятор в сборе
Свинцово-кислотный аккумулятор в сбореСвинцо́во-кисло́тный аккумуля́тор
Свинцовый аккумулятор изобрёл в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля[2]. В 1878 году Камилл Фор усовершенствовал его конструкцию, предложив покрывать пластины аккумулятора свинцовым суриком. Русский изобретатель Бенардос применил покрытие губчатым свинцом для увеличения мощности батарей, которые использовал в своих работах со сваркой.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в водном растворе серной кислоты.
При подключении к электродам аккумулятора внешней нагрузки начинается электрохимическая реакция взаимодействия оксида свинца и серной кислоты, при этом металлический свинец окисляется до сульфата свинца (в классическом варианте аккумулятора). Проведённые в СССР исследования показали, что при разряде аккумулятора протекает как минимум ~60 различных реакций, порядка 20 из которых протекают без участия кислоты электролита
Во время разряда происходит восстановление диоксида свинца на катоде[3][4] и окисление свинца на аноде. При заряде протекают обратные реакции. При перезаряде аккумулятора, после исчерпания сульфата свинца, начинается электролиз воды, при этом на аноде (положительный электрод) выделяется кислород, а на катоде — водород.
Электрохимические реакции (слева направо — при разряде, справа налево — при заряде):
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
При разряде аккумулятора из электролита расходуется серная кислота и выделяется относительно более лёгкая вода, плотность электролита падает. При заряде происходит обратный процесс. В конце заряда, когда количество сульфата свинца на электродах снижается ниже некоторого критического значения, начинает преобладать процесс электролиза воды. Газообразные водород и кислород выделяются из электролита в виде пузырьков — так называемое «кипение» при перезаряде. Это нежелательное явление, при заряде его следует по возможности избегать, так как при этом вода необратимо расходуется, нарастает плотность электролита и есть риск взрыва образующихся газов. Поэтому большинство зарядных устройств снижает зарядный ток при повышении напряжения аккумулятора. Потери воды восполняют доливкой в аккумуляторы дистиллированной воды при обслуживании аккумуляторной батареи (некоторые автомобильные батареи не имеют открывающихся/отвинчивающихся пробок)[5].
Элемент свинцово-кислотного аккумулятора состоит из электродов и разделительных пористых пластин, изготовленных из материала, не взаимодействующего с кислотой, препятствующих замыканию электродов (сепараторов), которые погружены в электролит. Электроды представляют собой плоские решётки из металлического свинца. В ячейки этих решёток запрессованы порошки диоксида свинца (PbO2) — в анодных пластинах и металлического свинца — в катодных пластинах. Применение порошков увеличивает поверхность раздела электролит — твердое вещество, тем самым увеличивает электрическую ёмкость аккумулятора.
Электроды вместе с сепараторами погружены в электролит, представляющий собой водный раствор серной кислоты. Для приготовления раствора кислоты применяют дистиллированную воду.
Электрическая проводимость электролита зависит от концентрации серной кислоты и при комнатной температуре максимальна при массовой доле кислоты 35%[6], что соответствует плотности электролита 1,26 г/см³[7]. Чем больше проводимость электролита, тем меньше внутреннее сопротивление аккумулятора, и, соответственно, ниже потери энергии на нём. Однако, на практике в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29−1,31 г/см³, это связано с тем, что при снижении концентрации из-за разряда электролит может замёрзнуть, а при замерзании образуется лёд, который может разорвать банки аккумулятора и повреждает губчатый материал пластин.
Существуют экспериментальные разработки аккумуляторов, где свинцовые решетки заменяют пластинами из переплетённых нитей углеродного волокна, покрытых тонкой свинцовой плёнкой. При этом используется меньшее количество свинца, распределённого по большой площади, что позволяет изготовить аккумулятор не только компактным и лёгким, при прочих равных параметрах, но и значительно более эффективным — помимо большего КПД, заряжается значительно быстрее традиционных аккумуляторов[8].
В аккумуляторах, применяемых в бытовых ИБП, систем охранной сигнализации и др. жидкий электролит загущают водным щелочным раствором силикатов натрия (Na2Si2O4) до пастообразного состояния. Это так называемые гелевые аккумуляторы (GEL), имеющие длительный ресурс. Другой вариант исполнения − с пористыми сепараторами из стеклоткани (AGM), допускающими более жёсткие режимы заряда[9].
Электрические и эксплуатационные параметры[править | править код]
- Удельная предельная теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 25—40[10].
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250[11].
- ЭДС одного заряжённого аккумулятора = 2,11—2,17 В, рабочее напряжение 2,1 В (3 или 6 аккумуляторов в итоге дают в батарее стандартные 6,3 В или 12,6 В соответственно)[3].
- Напряжение полностью разряженного аккумулятора = 1,75—1,8 В. Ниже разряжать их нельзя[3].
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80—90 % (по току). КПД по энергии 70-80%[10].
Чаще всего свинцово-кислотные аккумуляторы применяются в составе аккумуляторной батареи с номинальным напряжением 6, 12 вольт, реже с другим кратным 2 напряжением. Промышленностью выпускаются варианты обслуживаемых (заливание электролита, дистиллированной воды, контроль плотности электролита, его замена) и не обслуживаемых в герметичном корпусе (исключается проливание электролита при изменений положения, переворачиваний) аккумуляторных батарей. Обслуживаемые аккумуляторные батареи могут выпускаться сухозаряженными (без залитого электролита), что увеличивает их срок хранения и не требует периодического обслуживания при хранении, заливка производится перед вводом в эксплуатацию
Герметичная не обслуживаемая свинцово-кислотная аккумуляторная батарея напряжением 12 В и ёмкостью 4,5 А·ч бытовой электротехники
Свинцово-кислотные аккумуляторные батареи напряжением 8 В и ёмкостью 3,5 А·ч ИБП
Вариант обслуживаемой свинцово-кислотной аккумуляторной батареи для автомототракторной техники в эбонитовом корпусе, в подобных батареях была даже возможность заменить отдельный вышедший из строя аккумулятор
Вариант не обслуживаемой свинцово-кислотной аккумуляторной батареи для автомототракторной техники, нет доступа к заливным горловинам банок аккумуляторов
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде малым током (1/20 номинальной ёмкости, выраженной в А·ч)[13].
- Стартерный ток (для автомобильных аккумуляторов). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев измеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики замера отличаются (главным образом, допускаемым конечным напряжением) поэтому дают различные результаты[14].
- Резервная ёмкость
При эксплуатации «обслуживаемых» аккумуляторов (с открываемыми пробками на банках) на автомобиле при движении по неровной дороге неизбежно происходит просачивание электролита из-под пробок на корпус аккумулятора. Через электропроводную не высыхающую, из-за гигроскопичности, плёнку электролита происходит постепенный саморазряд аккумулятора. Во избежание глубокого саморазряда необходимо периодически нейтрализовать электролит протиранием корпуса аккумулятора, например, слабым раствором пищевой соды или разведённым в воде до консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита; также количество воды в электролите уменьшается при перезаряде аккумулятора за счёт её электролиза. Потеря воды увеличивает плотность электролита, увеличивая напряжение на аккумуляторе. При существенной потере воды могут оголиться пластины, что одновременно увеличивает саморазряд и вызывает сульфатацию батареи. Поэтому необходимо следить за уровнем электролита и при необходимости доливать дистиллированную воду.
Эти меры вместе с проверкой автомобиля на паразитную утечку тока в его электрооборудовании и периодической подзарядкой аккумулятора могут существенно продлить срок эксплуатации аккумуляторной батареи.
Работа свинцово-кислотного аккумулятора при низких температурах[править | править код]
По мере снижения окружающей температуры параметры аккумулятора ухудшаются, однако, в отличие от прочих типов аккумуляторов, у свинцово-кислотных аккумуляторов это снижение относительно мало, что и обуславливает их широкое применение на транспорте. Эмпирически считается, что свинцово-кислотный аккумулятор теряет ~1 % отдаваемой ёмкости при снижении температуры на каждый градус от +20 °C. То есть, при температуре −30 °C свинцово-кислотный аккумулятор покажет примерно 50 % ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, снижением скорости химических реакций (закон Аррениуса). Единственным способом повышения отдаваемой ёмкости является подогрев холодной батареи, как вариант — встроенным подогревателем (6СТ-190ТР-Н).
Разряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1,10 г/см3) и образования кристаллов льда, что приводит к необратимому повреждению свинцовых пластин внутри аккумулятора.
Низкие температуры электролита негативно влияют на работоспособность и зарядно-разрядные характеристики аккумулятора[16]:
- при температуре от 0 °C до −10 °C снижение зарядных и разрядных характеристик несущественно влияют на работоспособность аккумулятора;
- при температуре от −10 °C до −20 °C происходит снижение тока в стартерном режиме и ухудшение заряда;
- при температуре ниже −20 °C аккумуляторные батареи не обеспечивают надежного пуска двигателя и не способны принимать заряд от генератора.
Из-за большего внутреннего сопротивления, присущего современным аккумуляторам закрытого типа (т. н. «необслуживаемым», герметичным, герметизированным) при низких температурах по сравнению с обычными аккумуляторами (открытого типа), для них эти вопросы ещё более актуальны[17].
Для эксплуатации транспортных средств при очень низких температурах предназначены конструкции аккумулятора с внутренним электроподогревом
Хранение[править | править код]
Свинцово-кислотные аккумуляторы следует хранить только в заряженном состоянии. При температуре ниже −20 °C подзаряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/элемент 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/элемент в течение 6—12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи, солей и плёнки электролита на поверхности корпуса аккумулятора создаёт проводник для тока между электродами и приводит к саморазряду аккумулятора, при глубоком разряде начинается преждевременная сульфатация пластин, и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
При подготовке аккумуляторной батареи к зимнему хранению, что актуально для автомобилей не эксплуатируемых в холодное время года специалисты старейшей лаборатории НИИАЭ рекомендуют следующие действия:
1. Правильно и до конца зарядите аккумуляторную батарею. 2. Нанесите на положительный вывод АКБ пластичную смазку (литол, солидол и т. п.), так как плёнка электролита способна абсорбировать влагу из атмосферы, что может приводить к повышенному саморазряду. 3. Хранить аккумуляторы на холоде, так как при низких температурах саморазряд намного ниже. Электролит полностью заряженного аккумулятора начинает замерзать при температуре ниже −55 С.
В случае необходимости поездки в морозы следует перенести аккумулятор в отапливаемое помещение и в течение 7—9 часов (например, за ночь) он придёт в пригодное для пуска двигателя состояние.
Износ свинцово-кислотных аккумуляторов[править | править код]
При использовании технической серной кислоты и недистиллированной воды ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи[19].
При химических реакциях в аккумуляторе образуется плохо растворимое вещество — сульфат свинца PbSO4, осаждающийся на пластинах и создающий диэлектрический слой между электролитом и активной массой. Это один из факторов, снижающих срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[3], заключающаяся в образовании крупных кристаллов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения материала электродов в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с электродными решётками, что приводит к опаданию активной массы[3][20];
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности[3].
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, в домашних условиях восстановить нельзя, в литературе описаны химические растворы и прочие способы, позволяющие «десульфатировать» пластины. Простой, но чреватый полным отказом аккумулятора способ предполагает использование раствора сульфата магния[3]. Раствор сульфата магния заливается в секции, после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно банок, это может привести к замыканию элемента, поэтому обработанные банки желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства.
Кодовый символ, указывающий на то, что свинцовые батареи могут быть вторично переработаныВторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах, является токсичным тяжёлым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны для возможности его вторичного использования.
Свинец из изношенных аккумуляторов используется для кустарной переплавки, например, при изготовлении грузил рыболовных снастей, охотничьей дроби или гирь. Кустарное извлечение свинца из аккумуляторов серьезно вредит как окружающей среде, так и здоровью плавильщиков, поскольку свинец и его соединения с парами и дымом разносятся по всей округе[21][22].
- ↑ Курзуков Н. И., Ягнятинский В. М. Аккумуляторные батареи. Краткий справочник // М.: ООО «Книжное издательство „За рулём“». — 2008. — 88 с., ил. ISBN 978-5-9698-0236-0. (С. 15).
- ↑ Bertrand Gille Histoire des techniques. — Gallimard, coll. «La Pléiade», 1978, ISBN 978-2070108817.
- ↑ 1 2 3 4 5 6 7 8 Свинцовые аккумуляторы. Эксплуатация: Правда и вымыслы.
- ↑ Н. Ламтев. Самодельные аккумуляторы. Москва: Государственное издательство по вопросам радио, 1936 год.
- ↑ Как отрыть автомобильный аккумулятор: делаем батарею обслуживаемой (рус.), AkkumulyatorAvto.ru (2 августа 2017). Дата обращения 12 августа 2018.
- ↑ Удельная электропроводность х водных растворов серной кислоты и температурный коэффициент аt (неопр.). chemport.ru. Дата обращения 1 июля 2018.
- ↑ Концентрация и плотность серной кислоты. Зависимость плотности серной кислоты от концентрации в аккумуляторе автомобиля (рус.), FB.ru. Дата обращения 1 июля 2018.
- ↑ http://auto.lenta.ru/news/2006/12/19/battery/ Американцы облегчили и уменьшили аккумуляторы
- ↑ Аккумуляторы для бесперебойного питания. Статьи компании «ООО Новая система» (неопр.). aegmsk.ru. Дата обращения 12 августа 2018.
- ↑ 1 2 Свинцовый кислотный аккумулятор. Устройство и принцип действия аккумулятора. (рус.). www.eti.su. Дата обращения 1 июля 2018.
- ↑ Расчет идеального свинцового аккумулятора.
- ↑ [1].
- ↑ ГОСТ 26881-86 Методика проверки свинцовых аккумуляторов
- ↑ Краткий аналитический обзор существующих способов оценки ёмкости ХИТ и приборов, реализующих эти способы (неопр.) (недоступная ссылка). Дата обращения 21 октября 2011. Архивировано 4 марта 2016 года.
- ↑ ГОСТ Р 53165-2008: Батареи аккумуляторные свинцовые стартерные для автотракторной техники. Общие технические условия
- ↑ Руководство, 1983, с. 70.
- ↑ Железнодорожный транспорт. — 2011. № 12. — c.35. (неопр.) (недоступная ссылка). Дата обращения 13 декабря 2015. Архивировано 22 декабря 2015 года.
- ↑ Руководство, 1983, с. 21-23.
- ↑ Вредные добавки к электролиту свинцовых аккумуляторов
- ↑ О противоречиях в теории работы свинцового кислотного аккумулятора к. т. н., проф. Кочуров А. А. Рязанский военный автомобильный институт Архивировано 20 сентября 2011 года.
- ↑ Отравление свинцом | ProfMedik Медицинский Портал (рус.) (неопр.) ?. profmedik.ru (22 февраля 2016). Дата обращения 4 февраля 2017.
- ↑ Кочуров. http://echemistry.ru/assets/files/books/hit/statya-o-protivorechiyah-v-teorii-raboty-svincovogo-kislotnogo-akkumulyatora.pdf (рус.). Новости. Первоуральск.Ru (17 июля 2014). Дата обращения 4 февраля 2017.
ru.wikipedia.org
§42. Кислотные аккумуляторы
Принцип действия. Аккумулятором называется химический источник тока, который способен накапливать (аккумулировать) в себе электрическую энергию и по мере необходимости отдавать ее во внешнюю цепь. Накапливание в аккумуляторе электрической энергии происходит при пропускании по нему тока от
Рис. 158. Заряд (а) и разряд (б) аккумулятора
постороннего источника (рис. 158,а). Этот процесс, называемый зарядом аккумулятора, сопровождается превращением электрической энергии в химическую, в результате чего аккумулятор сам становится источником тока. При разряде аккумулятора (рис. 158, б) происходит обратное превращение химической энергии в электрическую. Аккумулятор обладает большим преимуществом по сравнению с гальваническим элементом. Если элемент разрядился, то он приходит в полную негодность; аккумулятор же. после разряда может быть вновь заряжен и будет служить источником электрической энергии. В зависимости от рода электролита аккумуляторы разделяют на кислотные и щелочные.
На локомотивах и электропоездах наибольшее распространение получили щелочные аккумуляторы, которые имеют значительно больший срок службы, чем кислотные. Кислотные аккумуляторы ТН-450 применяют только на тепловозах, они имеют емкость 450 А*ч, номинальное напряжение — 2,2 В. Аккумуляторная батарея 32 ТН-450 состоит из 32 последовательно соединенных аккумуляторов; буква Т означает, что батарея установлена на тепловозе, буква Н — тип положительных пластин (намазные).
Устройство. В кислотном аккумуляторе электродами являются свинцовые пластины, покрытые так называемыми активными массами, которые взаимодействуют с электролитом при электрохимических реакциях в процессе заряда и разряда. Активной массой положительного электрода (анода) служит перекись свинца PbO2, а активной массой отрицательного электрода (катода) — чистый (губчатый) свинец Pb. Электролитом является 25—34 %-ный водный раствор серной кислоты.
Пластины аккумулятора могут иметь конструкцию поверхностного или намазного типа. Пластины поверхностного типа отливают из свинца; поверхность их, на которой происходят электрохимические реакции, увеличена благодаря наличию ребер, борозд и т. п. Их применяют в стационарных аккумуляторных батареях и некоторых батареях пассажирских вагонов.
В аккумуляторных батареях тепловозов применяют пластины намазного типа (рис. 159, а). Такие пластины имеют остов из сплава свинца с сурьмой, в котором устроен ряд ячеек, заполняемых пастой.
Ячейки пластин после заполнения пастой закрывают свинцовыми листами с большим количеством отверстий. Эти листы предотвращают возможность выпадания из пластин активной массы и не препятствуют в то же время доступу к ней электролита.
Исходным материалом для изготовления пасты для положительных пластин служит порошок свинца Pb, а для отрицательных— порошок , перекиси свинца PbO2, которые замешиваются на водном растворе серной кислоты. Строение активных масс в таких пластинах пористое; благодаря этому в электрохимических реакциях участвуют не только поверхностные, но и глубоколежащие слои электродов аккумулятора.
Для повышения пористости и уменьшения усадки активной массы в пасту добавляют графит, сажу, кремний, стеклянный порошок, сернокислый барий и другие инертные материалы, называемые расширителями. Они не принимают участия в электрохимических реакциях, но затрудняют слипание (спекание) частиц свинца и его окислов и предотвращают этим уменьшение пористости.
Намазные пластины имеют большую поверхность соприкосновения с электролитом и хорошо им пропитываются, что способствует уменьшению массы и размеров аккумулятора и позволяет получать при разряде большие токи.
Рис. 159. Устройство пластин (а) и общий вид (б) кислотного аккумулятора: 1 — блок намазных отрицательных пластин; 2 — выводные штыри; 3 — блок панцирных положительных пластин; 4 — панцирь; 5 — активная масса; 6 — отверстие с пробкой для заливки электролита; 7 — крышка; 8 — эбонитовый сосуд; 9 — пространство для осаждения шлама
При изготовлении аккумуляторов пластины подвергают специальным зарядно-разрядным циклам. Этот процесс носит название формовки аккумулятора. В результате формовки паста положительных пластин электрохимическим путем превращается в перекись (двуокись) свинца PbO2 и приобретает коричневый цвет. Паста отрицательных пластин при формовке переходит в чистый свинец Pb, имеющий пористую структуру и называемый поэтому губчатым; отрицательные пластины приобретают серый цвет.
В некоторых аккумуляторах применены положительные пластины панцирного типа. В них каждая положительная пластина заключена в специальный панцирь (чехол) из эбонита или стеклоткани. Панцирь надежно удерживает активную массу пластины от осыпания при тряске и толчках; для сообщения же активной массы пластин с электролитом в панцире делают горизонтальные прорези шириной около 0725 мм.
Для предотвращения замыкания пластин посторонними предметами (щупом для измерения уровня электролита, устройством для заливки электролита и др.) пластины в некоторых аккумуляторах покрывают полихлорвиниловой сеткой.
Для увеличения емкости в каждый аккумулятор устанавливают несколько положительных и отрицательных пластин; одноименные пластины соединяют параллельно в общие блоки, к которым приваривают выводные штыри. Блоки положительных и отрицательных пластин обычно устанавливают в эбонитовом аккумуляторном сосуде (рис. 159,б) так, чтобы между каждыми двумя
Рис. 160. Прохождение через электролит положительных и отрицательных ионов при разряде (а) и заряде (б) кислотного аккумулятора
пластинами одной полярности располагались пластины другой полярности. По краям аккумулятора ставят отрицательные пластины, так как положительные пластины при установке по краям склонны к короблению. Пластины отделяют одну от другой сепараторами, выполненными из микропористого эбонита, полихлорвинила, стекловойлока или другого изоляционного материала. Сепараторы предотвращают возможность короткого замыкания между пластинами при их короблении.
Пластины устанавливают в аккумуляторном сосуде так, чтобы между их нижней частью и дном сосуда имелось некоторое свободное пространство. В этом пространстве скапливается свинцовый осадок (шлам), образующийся вследствие отпадания отработавшей активной массы пластин в процессе эксплуатации.
Разряд и заряд. При разряде аккумулятора (рис. 160, а) положительные ионы H2+ и отрицательные ионы кислотного остатка
S04-, на которые распадаются молекулы серной кислоты H2S04 электролита 3, направляются соответственно к положительному
1 и отрицательному 2 электродам и вступают в электрохимические реакции с их активными массами. Между электродами возникает
разность потенциалов около 2 В, обеспечивающая прохождение электрического тока при замыкании внешней цепи. В результате
электрохимических реакций, возникающих при взаимодействии ионов водорода с перекисью свинца PbO2 положительного
электрода и ионов сернокислого остатка S04— со свинцом Pb отрицательного электрода, образуется сернокислый свинец PbS04 (сульфат свинца), в который превращаются поверхностные слои активной массы обоих электродов. Одновременно при этих реакциях образуется некоторое количество воды, поэтому концентрация серной кислоты понижается, т. е. плотность электролита уменьшается.
Аккумулятор может разряжаться теоретически до полного превращения активных масс электродов в сернокислый свинец и истощения электролита. Однако практически разряд прекращают гораздо раньше. Образующийся при разряде сернокислый свинец представляет собой соль белого цвета, плохо растворяющуюся в электролите и обладающую низкой электропроводностью. Поэтому разряд ведут не до конца, а только до того момента, когда в сернокислый свинец перейдет около 35 % активной массы. В этом случае образовавшийся сернокислый свинец равномерно распределяется в виде мельчайших кристалликов в оставшейся активной массе, которая сохраняет еще достаточную электропроводность, чтобы обеспечить напряжение между электродами 1,7—1,8 В.
Разряженный аккумулятор подвергают заряду, т. е. присоединяют к источнику тока с напряжением, большим напряжения аккумулятора. При заряде (рис. 160,б) положительные ионы водорода перемещаются к отрицательному электроду 2, а отрицательные ионы сернокислого остатка S04— — положительному электроду 1 и вступают в химическое взаимодействие с сульфатом свинца PbS04, покрывающим оба электрода. В процессе возникающих электрохимических реакций сульфат свинца PbS04 растворяется и на электродах вновь образуются активные массы: перекись свинца PbO2 на положительном электроде и губчатый свинец Pb — на отрицательном. Концентрация серной кислоты при этом возрастает, т. е. плотность электролита увеличивается.
Электрохимические реакции при разряде и заряде аккумулятора могут быть выражены уравнением
PbO2 + Pb + 2H2SO4 ? 2PbSO4 + 2H2O
Читая это уравнение слева направо, получаем процесс разряда, справа налево — процесс заряда.
Номинальный разрядный ток численно равен 0,1СНОМ, максимальный при запуске дизеля (стартерный режим) — примерно 3СНОМ, зарядный ток — 0,2 СНОМ, где СНОМ — номинальная емкость.
Полностью заряженный аккумулятор имеет э. д. с. около 2,2 В. Таково же приблизительно и напряжение на его зажимах, так как внутреннее сопротивление аккумулятора весьма мало. При разряде напряжение аккумулятора довольно быстро падает до 2 В, а затем медленно понижается до 1,8—1,7 В (рис. 161), при этом напряжении разряд прекращают во избежание повреждения аккумулятора. Если разряженный аккумулятор оставить на некоторое время в бездействии, то напряжение его снова восстанавливается до среднего значения 2 В. Это явление носит название «отдыха» аккумулятора. При нагрузке подобного «отдохнувшего» аккумулятора напряжение быстро понижается, поэтому измерение напряжения аккумулятора без нагрузки не дает правильного суждения о степени разряда.
При заряде напряжение аккумулятора быстро поднимается до 2,2 В, а затем медленно повышается до 2,3 В и, наконец, снова довольно быстро возрастает до 2,6—2,7 В. При 2,4 В начинают выделяться пузырьки газа, образующегося в результате разложения воды на водород и кислород. При 2,5 В оба электрода выделяют сильную струю газа, а при 2,6—2,7 В аккумулятор начинает как бы кипеть, что служит признаком окончания заряда. При отключении аккумулятора от источника зарядного тока напряжение его быстро снижается до 2,2 В.
Уход за аккумуляторами. Кислотные аккумуляторы быстро теряют емкость или даже приходят в полную негодность при
Рис. 161. Кривые напряжения кислотного аккумулятора при заряде и разряде
неправильной эксплуатации. В них происходит саморазряд, в результате которого они теряют свою емкость (примерно 0,5— 0,7 % в сутки). Для компенсации саморазряда неработающие аккумуляторные батареи необходимо периодически подзаряжать. При загрязнении электролита, а также крышек аккумуляторов, их выводов и междуэлементных соединений происходит повышенный саморазряд, быстро истощающий батарею.
Батарея аккумулятора должна быть всегда чистой, а выводы для предохранения от окисления покрыты тонким слоем технического вазелина. Периодически нужно проверять уровень электролита и степень заряженности аккумуляторов. Аккумуляторы должны периодически заряжаться. Хранение незаряженных аккумуляторов недопустимо. При неправильной эксплуатации аккумуляторов (разряде ниже 1,8—1,7 В, систематическом недозаряде, неправильном проведении заряда, длительном хранении незаряженного аккумулятора, понижении уровня электролита, чрезмерной плотности электролита) происходит повреждение их пластин, называемое сульфатацией. Это явление заключается в переходе мелкокристаллического сульфата свинца, покрывающего пластины при разряде, в нерастворимые крупнокристаллические химические соединения, которые при заряде не переходят в перекись свинца РbO2 и свинец РЬ. При этом аккумулятор становится непригодным для эксплуатации.
electrono.ru
Кислотные аккумуляторы: конструкция, характеристики
Аккумулятор — источник питания, в котором при разряде энергия химической реакции преобразовывается в электрическую, а при заряде — наоборот. Главное отличие от обычной батареи – это возможность восстановления энергии методом повторной зарядки. Для заряда нужно подключить постоянный ток в направлении, обратном разряду.
Кислотные аккумуляторы были изобретены в 19 веке, но до сих пор являются самыми востребованными в мире благодаря невысокой стоимости и высокой степени эффективности. Устройство состоит из корпуса, двух разнополярных электродов, помещенных в электролит – раствор кислоты, от этого получено название – кислотные батареи (АКБ — Аккумуляторные Кислотные Батареи). По материалу, из которого изготовлены электроды, их еще называют свинцово-кислотные.

Как работают?
Основой работы аккумулятора является электрохимический процесс взаимодействия свинца и диоксида свинца в водном растворе серной кислоты. При включении нагрузки на электроды происходит химическая реакция диоксида свинца с серной кислотой H2SO4, а также реакция окисления свинца до сульфата свинца. В процессе разряда на катоде («-») идет восстановление диоксида свинца, на аноде («+») — окисление свинца. Во время зарядки происходят обратные химические реакции и электролиз воды с выделением кислорода на аноде, водорода на катоде.
Реакции взаимодействия, протекающие в аккумуляторе, можно описать двумя формулами:
- PbO2 + Pb + 2H2SO4 → 2PbSO4 + 2H2O – разряд.
- 2PbSO4 + 2H2O → PbO2 + Pb + 2H2SO4 — заряд.
При разрядке идет процесс образования сульфата свинца в активных массах анода и катода, расходование серной кислоты H2SO4 и снижение плотности электролита. Во время зарядки происходят обратные реакции, идет образование серной кислоты, повышается плотность электролита. Окончание процесса заряда характеризуется завершением преобразования веществ на электродах, прекращением изменения электролита. Если продолжать зарядку, то возникает нежелательная реакция разложения воды (электролиз), идет выделение кислородных и водородных пузырьков в электролите, происходит иллюзия закипания. Если это произошло, необходимо добавить в аккумулятор дистиллированной воды для восстановления ее в электролите.
Конструкция
Кислотные батареи уже более ста лет не меняются по своему основному внутреннему устройству.
В конструкцию аккумуляторных батарей входят:
- Электроды – в виде плоских решеток из свинца, в ячейки запрессован порошок диоксид свинца (PbO2) на аноде, порошок металлического свинца (Pb) — на катоде.
- Сепаратор — пористый диэлектрик, разделяет между собой электроды, препятствуя замыканию.
- Электролит — разбавленная водой (дистиллированной) серная кислота H2SO4, в нее помещены электроды и сепаратор. Максимальная электропроводность достигается при температуре 20оС, концентрации серной кислоты – 35 %, что означает плотность электролита 1,26 г/см³. Внутренне сопротивление при этом минимально, потери внутри устройства существенно малы. В местах с низкотемпературным климатом возможно повышение плотности раствора до 1,29 г/см³ – 1,31 г/см³. Увеличение концентрации кислотного раствора препятствует замерзанию электролита, образованию льда внутри корпуса, который может повредить электроды и разорвать аккумулятор.
Основные характеристики, параметры
- Емкость (номинальная) — количество электрической энергии, которое могут дать кислотные батареи, измерение происходит в момент разряда, при нагрузке маленьким током потребления, единицы измерения— А*ч.
- Стартерный ток – показывает способность АКБ отдавать большие токи при температуре — 18оС на протяжении половины минуты.
- Емкость(резервная) — показывает временной промежуток, на протяжении которого кислотные батареи отдают ток 25 А до величины напряжения 10,5 В.
- Нижнее значение напряжения разряженной АКБ — 1,75 — 1,8 V.
- Температурный рабочий диапазон — – 40ос — + 40оС.
Разновидности
По режиму работы кислотные батареи можно разделить на три группы:
- Циклический — принцип работы происходит по циклу – полный разряд — полный заряд, периодически отключается от источника питания. Считается наиболее жестким режимом, количество циклов стопроцентной разрядки ограничено.
- Буферный — широко используемый режим, щадящий для АКБ, при нем не допускается полного разряда, характерно постоянное подключение к источнику питания.
- Смешанный — комбинация буферного и циклических режимов, но большая часть времени работы проходит в буферном.
Самые распространенные кислотные батареи, представленные на рынке, можно разделить на виды:
| Вид | Обслуживание | Описание | Вольтаж, V |
| Lead-Acid | Обслуживаемые | Автомобильные АКБ, бывают: малосурьмянистые, сурьмянистые, кислотно-кальциевые, гибридные. | 612 |
| AGM VRLA | Не требуют обслуживания | Сепараторы изготовлены из стекловолокна, циклический и буферный режим работы. | 24612 |
| VRLA | Не требуют обслуживания | Герметичный корпус, бывают кальциевые, не выделяют газов, используются в буферном режиме. | 24612 |
| GEL VLRA | Не требуют обслуживания | В качестве электролита — селикагель, что продлевает срок службы АКБ, буферный режим эксплуатации. | 24612243648 |
| OPzV | Не требуют обслуживания | Электроды трубчатой конструкции, устойчивы к полному разряду, срок службы — около 22 лет. | 2 |
Применение
- Автотранспорт — кислотные батареи используются как стартерные батареи.
- Компьютерная техника — источники бесперебойного питания (ИБП) позволяют сохранить информацию в случае аварийного отключения электричества.
- Промышленное производство — кислотные батареи используются как источники резервного питания.
Зарядка и общие рекомендации
- Зарядку необходимо проводить при температуре 20оС.
- Ток заряда не должен превышать 10 % номинального значения емкости АКБ.
- Для использования в транспортных средствах кислотные батареи при низких температурах, лучше применять с системой внутреннего электроподогрева, т. к. емкость устройства теряется на 1% при снижении температуры на 1оС.
- Не рекомендуется хранить кислотные батареи при температуре выше 30оС, либо разряженными, предварительно АКБ должны быть полностью заряжены.
- Хранение зимой лучше организовать на холоде, т. к. процесс саморазряда будет минимален, и на плюсовую клемму необходимо предварительно нанести солидол.
- Перед использованием, кислотные батареи нужно занести в помещение с температурой 20оС на 8-10 часов для приведения в рабочее состояние.
batareykaa.ru
Кислотные аккумуляторы; чтобы больше не было отвратительно читать то что люди о них пишут
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить.Начнем с названия. Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там.
С химической точки зрения любые АКБ абсолютно одинаковы. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:
Тут мы видим, что в форсированном режиме напряжение заряда может быть аж 15В.
Все разъяснит кривая напряжения на АКБ:
Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
1 Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
2 Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
3 Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды. Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2H2O = 2H2 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции. Про них бытуют следующие мифы:
1. Водород крайне взрывоопасен! Перезарядишь аккумулятор и как минимум лишишься комнаты где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты. Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества h3 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства. Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2. При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
3. При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги. Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду. Процедура доливания воды — необходимая часть процесса обслуживания любой АКБ. Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т.н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + SiO2 + H2O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
1. Малогабаритные и крупногабаритные АКБ идентичны по устройству.
2. Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
3. Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
4. Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
5. Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
6. Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
habr.com
Свинцово кислотный аккумулятор — принцип работы, как правильно заряжать
Свинцово-кислотный аккумулятор – один из самых надёжных АКБ, разработанный ещё в XIX веке, но до сих пор используемый во многих областях. В его основе лежит химическая реакция с переносом электронов от анода к катоду. Аккумулятор со временем портится при разрядке-подзарядке, так что данный процесс должен выполняться по всем правилам, чтобы продлить жизнь батареи.
Устройство и принцип работы свинцово-кислотного аккумулятора
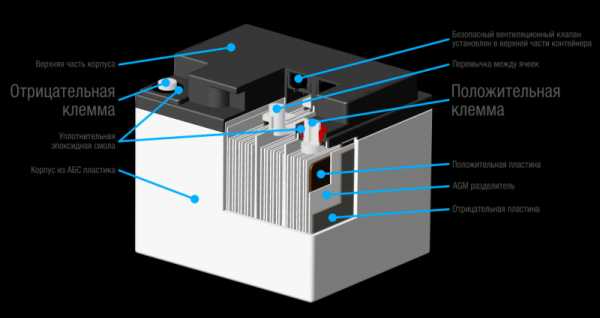
Данный тип стационарного АКБ довольно тяжёлый, так как состоит из плотно параллельно упакованных плёнок свинца и оксида свинца. И те и другие в аккумуляторе расположены очень густо. Свинцовые пластины тёмно-серого цвета с синим оттенком, оксидно-свинцовые – тёмно-коричневые с рыжим оттенком.
Обе пластины находятся в серной кислоте, из-за чего в названии АКБ есть соответствующее слово. При включении аккумулятора ток протекает от оксидно-свинцового катода к свинцовому аноду. При этом свинец выделяет электроны, которые оксид свинца принимает.
В результате изменения заряда двух пластин они вступают в реакцию с серной кислотой вокруг и превращаются в сульфаты свинца.
Pb + HSO4– => PbSO4 + H+ + 2e–
PbO2 + HSO4– + 3H+ + 2e– => PbSO4 + 2h3O
Пара пластин производит 2 вольта, поэтому, чтобы увеличить количество вольт, которое может дать аккумулятор, пластины соединяют параллельно во множество пар слоёв. Они упаковываются плотно в банку, чтобы уменьшить объём батареи. Но так как электроны должны передаваться через терминалы, то пары пластин разъединяются специальными изоляционными плёнками.
При этом аккумулятор может иметь либо высокую плотность энергии, либо мощности. То есть аккумулятор или сохраняет большое количество энергии и отдаёт её в течение длительного времени, или он отдаёт огромный заряд очень быстро. В автомобилях используется второй вариант, так как надо отдать более 400 ампер, чтобы завести двигатель.
При глубокой разрядке батареи на пластинах образуется налёт сульфата свинца. Именно из-за этого если посадить аккумулятор до нулевого заряда несколько раз, то можно просто уничтожить его. Сульфат свинца полностью покрывает поверхность пластин, после чего его уже невозможно будет зарядить.
Типы и особенности свинцово-кислотных АКБ

Идеальных аккумуляторов не существует, в инженерных конструкциях часто приходится жертвовать желаемыми характеристиками, чтобы получить необходимые параметры. Для каждой цели создан свой тип устройства.
В первую очередь АКБ делят на герметичные и негерметичные батареи. Вторые требуют постоянного контроля над уровнем электролита и состоянием катодов и анодов, могут работать лишь в определённых положениях. Аккумулятор герметичный свинцово-кислотный используется чаще, так как не нуждается в особом уходе.
Кроме того, все батареи можно разделить на следующие группы:
- Стартерные. Выдают большое количество энергии за одно мгновение, из-за чего обладают большим саморазрядом. Отлично подходят для того, чтобы заводить автомобили. Требуют определённого обслуживания и вентиляции.
- Буферные батареи. Предназначены для краткосрочного хранения небольшого количества энергии, работают в постоянном режиме подзарядки.
- Аккумуляторы для бесперебойной аппаратуры. Устанавливаются в офисах для аварийного завершения работ.
- Аккумуляторы длительного электроснабжения. Большие тяжёлые батареи, которые выдают достаточно много энергии длительное время. Используются в реанимационных отделениях на случай отключения электричества.
- Гелевые аккумуляторы. Хорошо переносят циклы заряжения-разряжения. Благодаря этому могут использоваться в сильных морозах. Среди них отдельно можно выделить солнечные батареи, которые рассчитаны на многократные циклы.
Как достигается такая вариация характеристик свинцово-кислотных аккумуляторных батарей? Если требуется выдавать огромное количество энергии за короткое время, то пластины делаются тонкими, но высокими и широкими (больше по площади поверхности), а расстояние между ними уменьшается. Благодаря этому увеличивается соотношение поверхности и массы, в результате энергия отдаётся быстрее.
Если требуется дольше сохранять энергию, но можно уменьшить мощность, то пластины делаются толще, но короче и уже (меньше по площади поверхности), а расстояние между ними увеличивается. Из-за чего уменьшается соотношение поверхности и массы, в итоге электроэнергия отдаётся медленнее.
Кроме того, на свойства аккумулятора влияют характеристики электролита и другие параметры. Гелевые электролиты хуже реагируют со свинцовыми и оксидно-свинцовыми плитами, а также делают конструкцию защищённой от вытекания. Повышает срок эксплуатации использование свинцово-кальциевых сплавов.
Области применения свинцово-кислотных аккумуляторов
Свинцово-кислотные аккумуляторы используются повсеместно, так как свинец и его оксид отвечают наиболее важным требованиям:
- элементы часто встречаются в природе и довольно легко добываются;
- они в паре способны накапливать и отдавать энергию лучше, чем все другие элементы;
- аккумуляторы из них просты и дешевы в производстве;
- долгий срок службы, возможность многократной перезарядки;
- простое обслуживание, что особенно характерно для герметичных конструкций.
Из-за этого батареи применяются в следующих областях:
- сигнализационные системы;
- стартёры в автомобилях;
- системы пожарной безопасности;
- системы аварийной подачи электроэнергии на телевидении, в реанимационных отделениях;
- электрические весы и кассовые аппараты;
- системы бесперебойного электроснабжения или аварийного отключения в компьютерной технике или их сетях;
- детские игрушки;
- в лёгких самолётах.
Тем не менее, имеются некоторые минусы:
- аккумуляторы чувствительны с холоду;
- отходы из них опасны для экологии;
- количество циклов довольно ограничено;
- есть лимиты у выдаваемой мощности.
Как правильно заряжать свинцово-кислотные аккумуляторы

Принцип зарядки состоит в том, что нужно изменить направление тока. Из-за этого электролит и материя двух пластин восстанавливает свой прежний химический состав. Данный процесс именуется циклом, и он может быть многократным. Но чтобы не повредить и продлить срок службы батареи, надо знать, как правильно заряжать свинцово-кислотный аккумулятор.
Важно! Для процедуры потребуется источник тока и устройство, которым можно регулировать силу тока и напряжение.
Прежде всего, нужно знать параметры аккумулятора, которые можно посмотреть на самой коробке устройства. Производители часто указывают информацию на английском языке. Обозначается всё это следующим образом:
| На английском | На русском |
| 12V | 12 вольт |
| 7.2Ah | 7.2 ампер-часов |
Также производитель может указывать напрямую, каким током можно заряжать аккумулятор:
| На английском | На русском |
| Standby use – 13.5-13,8V | Если вы используете батарею, как резервный источник электричества – 13,5-13,8 вольт |
| Cycle use – 14.4V | Если вы его применяете в качестве стартёра, то есть циклическое использование – 14.4 вольт |
| 2.16A MAX | При любой зарядке ток не должен превышать 2.16 ампера |
А что если производитель не указал, каким током заряжать аккумулятор? В этом случае можно пользоваться простым правилом – напряжение не должно превышать 10% от его номинальной ёмкости. То есть если у батареи указан параметр 7.2Ah, то заряжать надо при 0.72A.
После того как разобрались с основными параметрами, нужно сделать прибор, которым можно зарядить аккумулятор. Для этого потребуется крепкая коробка (лучше пластиковая) с отверстиями для вентиляции, блок питания от ноутбука, плата для регулировки тока и напряжения.
Дополнительно можно встроить многооборотистые переменные резисторы для более тонкой настройки, а также вольтамперметр. Для зарядки автомобильных аккумуляторов потребуется понижающий преобразователь напряжения и более мощный блок питания.
Собрав конструкцию, можно переходить непосредственно к главной процедуре. Для начала на неподключенном к аккумулятору устройстве нужно выставить напряжение, которым надо заряжать АКБ. Далее необходимо убавить силу тока до минимума, в результате чего сразу же упадёт напряжение. После этого подключаем устройство к аккумулятору (плюс к плюсу, минус к минусу).
В этот момент вольтамперметр будет показывать напряжение, которое есть на батарее. Включаем устройство в розетку и поднимаем силу тока до необходимой величины (метод её расчёта описан выше). В этот момент возможно незначительное снижение напряжения, говорящее о том, что ток уходит на прогрев электролита и преодоление сопротивления аккумулятора. Это нормально.
К концу зарядки аккумулятора сила тока на вольтамперметре будет практически равна нулю.
3batareiki.ru
Свинцово-кислотный аккумулятор — Википедия
Свинцо́во-кисло́тный аккумуля́тор — тип аккумуляторов, получивший широкое распространение ввиду умеренной цены, неплохого ресурса (от 500 циклов и более), высокой удельной мощности. Основные области применения: стартерные аккумуляторные батареи в транспортных средствах, аварийные источники электроэнергии, резервные источники энергии. Строго говоря, аккумулятором называется один элемент аккумуляторной батареи, но в просторечии «аккумулятором» называют аккумуляторную батарею (сколько бы в ней не было элементов).
История
Свинцовый аккумулятор изобрёл в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля[1]. В 1878 году Камилл Фор усовершенствовал его конструкцию, предложив покрывать пластины аккумулятора свинцовым суриком. Русский изобретатель Бенардос применил покрытие губчатым свинцом для увеличения мощности батарей, которые использовал в своих работах со сваркой.
Принцип действия
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в водном растворе серной кислоты.
При подключении к электродам аккумулятора внешней нагрузки начинается электрохимическая реакция взаимодействия оксида свинца и серной кислоты, при этом металлический свинец окисляется до сульфата свинца (в классическом варианте аккумулятора). Проведенные в СССР исследования показали, что при разряде аккумулятора протекает как минимум ~60 различных реакций, порядка 20 из которых протекают без участия кислоты электролита[2].
Во время разряда происходит восстановление диоксида свинца на катоде[2][3] и окисление свинца на аноде. При заряде протекают обратные реакции. При перезаряде аккумулятора, после исчерпания сульфата свинца, начинается электролиз воды, при этом на аноде (положительный электрод) выделяется кислород, а на катоде — водород.
Электрохимические реакции (слева направо — при разряде, справа налево — при заряде):
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
При разряде аккумулятора из электролита расходуется серная кислота и выделяется относительно более лёгкая вода, плотность электролита падает. При заряде происходит обратный процесс. В конце заряда, когда количество сульфата свинца на электродах снижается ниже некоторого критического значения, начинает преобладать процесс электролиза воды. Газообразные водород и кислород выделяются из электролита в виде пузырьков — так называемое «кипение» при перезаряде. Это нежелательное явление, при заряде его следует по возможности избегать, так как при этом вода необратимо расходуется, нарастает плотность электролита и есть риск взрыва образующихся газов. Поэтому большинство зарядных устройств снижает зарядный ток при повышении напряжения аккумулятора. Потери воды восполняют доливкой в аккумуляторы дистиллированной воды при обслуживании аккумуляторной батареи (некоторые автомобильные батареи не имеют открывающихся/отвинчивающихся пробок)[4].
Устройство

Элемент свинцово-кислотного аккумулятора состоит из электродов и разделительных пористых пластин, изготовленных из материала, не взаимодействующего с кислотой, препятствующих замыканию электродов (сепараторов), которые погружены в электролит. Электроды представляют собой плоские решётки из металлического свинца. В ячейки этих решёток запрессованы порошки диоксида свинца (PbO2) — в анодных пластинах и металлического свинца — в катодных пластинах. Применение порошков увеличивает поверхность раздела электролит — твердое вещество, тем самым увеличивает электрическую ёмкость аккумулятора.
Электроды вместе с сепараторами погружены в электролит, представляющий собой водный раствор серной кислоты. Для приготовления раствора кислоты применяют дистиллированную воду.
Электрическая проводимость электролита зависит от концентрации серной кислоты и при комнатной температуре максимальна при массовой доле кислоты 35%[5], что соответствует плотности электролита 1,26 г/см³[6]. Чем больше проводимость электролита, тем меньше внутреннее сопротивление аккумулятора, и, соответственно, ниже потери энергии на нём. Однако, на практике в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29−1,31 г/см³, это связано с тем, что при снижении концентрации из-за разряда электролит может замёрзнуть, а при замерзании образуется лёд, который может разорвать банки аккумулятора и повреждает губчатый материал пластин.
Существуют экспериментальные разработки аккумуляторов, где свинцовые решетки заменяют пластинами из переплетённых нитей углеродного волокна, покрытых тонкой свинцовой пленкой. При этом используется меньшее количество свинца, распределённого по большой площади, что позволяет изготовить аккумулятор не только компактным и лёгким, при прочих равных параметрах, но и значительно более эффективным — помимо большего КПД, заряжается значительно быстрее традиционных аккумуляторов[7].
В аккумуляторах, применяемых в бытовых ИБП, систем охранной сигнализации и др. жидкий электролит загущают водным щелочным раствором силикатов натрия (Na2Si2O4) до пастообразного состояния. Это так называемые гелевые аккумуляторы (GEL), имеющие длительный ресурс. Другой вариант исполнения − с пористыми сепараторами из стеклоткани (AGM), допускающими более жёсткие режимы заряда[8].
Электрические и эксплуатационные параметры
- Удельная предельная теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 30—40[9].
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250[10].
- ЭДС одного элемента заряжённого аккумулятора = 2,11—2,17 В, рабочее напряжение 2 В (3 или 6 секций в итоге дают стандартные 6 В или 12 В соответственно)[2].
- Напряжение полностью разряженного аккумулятора = 1,75—1,8 В (на 1 элемент). Ниже разряжать их нельзя[2].
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80—90 % (по току). КПД по энергии 70-80%[11].
Эксплуатационные характеристики
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде малым током (1/20 номинальной ёмкости, выраженной в А·ч)[12].
- Стартерный ток (для автомобильных аккумуляторов). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев измеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики замера отличаются (главным образом, допускаемым конечным напряжением) поэтому дают различные результаты[13].
- Резервная ёмкость (для автомобильных аккумуляторов) — характеризует время, в течение которого аккумулятор может отдавать ток 25 А до конечного напряжения 10,5 В согласно ГОСТ Р 53165-2008[14].
Эксплуатация
Ареометр может быть использован для проверки плотности электролита в каждом отдельном элементеПри эксплуатации «обслуживаемых» аккумуляторов (с открываемыми пробками на банках) на автомобиле при движении по неровной дороге неизбежно происходит просачивание электролита из-под пробок на корпус аккумулятора. Через электропроводную не высыхающую, из-за гигроскопичности, пленку электролита происходит постепенный саморазряд аккумулятора. Во избежание глубокого саморазряда необходимо периодически нейтрализовать электролит протиранием корпуса аккумулятора, например, слабым раствором пищевой соды или разведенным в воде до консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита; также количество воды в электролите уменьшается при перезаряде аккумулятора за счёт её электролиза. Потеря воды увеличивает плотность электролита, увеличивая напряжение на аккумуляторе. При существенной потере воды могут оголиться пластины, что одновременно увеличивает саморазряд и вызывает сульфатацию батареи. Поэтому необходимо следить за уровнем электролита и при необходимости доливать дистиллированную воду.
Эти меры вместе с проверкой автомобиля на паразитную утечку тока в его электрооборудовании и периодической подзарядкой аккумулятора могут существенно продлить срок эксплуатации аккумуляторной батареи.
Работа свинцово-кислотного аккумулятора при низких температурах
По мере снижения окружающей температуры параметры аккумулятора ухудшаются, однако, в отличие от прочих типов аккумуляторов, у свинцово-кислотных аккумуляторов это снижение относительно мало, что и обуславливает их широкое применение на транспорте. Эмпирически считается, что свинцово-кислотный аккумулятор теряет ~1 % отдаваемой ёмкости при снижении температуры на каждый градус от +20 °C. То есть, при температуре −30 °C свинцово-кислотный аккумулятор покажет примерно 50 % ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, снижением скорости химических реакций (закон Аррениуса). Единственным способом повышения отдаваемой ёмкости является подогрев холодной батареи, как вариант — встроенным подогревателем (6СТ-190ТР-Н).
Разряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1,10 г/см3) и образования кристаллов льда, что приводит к необратимому повреждению свинцовых пластин внутри аккумулятора.
Низкие температуры электролита негативно влияют на работоспособность и зарядно-разрядные характеристики аккумулятора[15]:
- при температуре от 0 °C до −10 °C снижение зарядных и разрядных характеристик несущественно влияют на работоспособность аккумулятора;
- при температуре от −10 °C до −20 °C происходит снижение тока в стартерном режиме и ухудшение заряда;
- при температуре ниже −20 °C аккумуляторные батареи не обеспечивают надежного пуска двигателя и не способны принимать заряд от генератора.
Из-за большего внутреннего сопротивления, присущего современным аккумуляторам закрытого типа (т. н. «необслуживаемым», герметичным, герметизированным) при низких температурах по сравнению с обычными аккумуляторами (открытого типа), для них эти вопросы ещё более актуальны[16].
Для эксплуатации транспортных средств при очень низких температурах предназначены конструкции аккумулятора с внутренним электроподогревом[17].
Хранение
Свинцово-кислотные аккумуляторы следует хранить только в заряженном состоянии. При температуре ниже −20 °C подзаряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/элемент 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/элемент в течение 6—12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи, солей и плёнки электролита на поверхности корпуса аккумулятора создаёт проводник для тока между электродами и приводит к саморазряду аккумулятора, при глубоком разряде начинается преждевременная сульфатация пластин, и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
При подготовке аккумуляторной батареи к зимнему хранению, что актуально для автомобилей не эксплуатируемых в холодное время года специалисты старейшей лаборатории НИИАЭ рекомендуют следующие действия:
1. Правильно и до конца зарядите аккумуляторную батарею. 2. Нанесите на положительный вывод АКБ пластичную смазку (литол, солидол и т. п.), так как плёнка электролита способна абсорбировать влагу из атмосферы, что может приводить к повышенному саморазряду. 3. Хранить аккумуляторы на холоде, так как при низких температурах саморазряд намного ниже. Электролит полностью заряженного аккумулятора начинает замерзать при температуре ниже −55 С.
В случае необходимости поездки в морозы следует перенести аккумулятор в отапливаемое помещение и в течение 7—9 часов (например, за ночь) он придёт в пригодное для пуска двигателя состояние.
Износ свинцово-кислотных аккумуляторов
При использовании технической серной кислоты и недистиллированной воды ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи[18].
При химических реакциях в аккумуляторе образуется плохо растворимое вещество — сульфит свинца PbSO3, осаждающийся на пластинах и который образует диэлектрический слой между электролитом и активной массой. Это один из факторов, снижающих срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[2], заключающаяся в образовании крупных кристаллов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения материала электродов в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с электродными решётками, что приводит к опаданию активной массы[2][19];
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности[2].
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, в домашних условиях восстановить нельзя, в литературе описаны химические растворы и прочие способы, позволяющие «десульфатировать» пластины. Простой, но чреватый полным отказом аккумулятора способ предполагает использование раствора сульфата магния[2]. Раствор сульфата магния заливается в секции, после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно банок, это может привести к замыканию элемента, поэтому обработанные банки желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства.
Вторичная переработка
Кодовый символ, указывающий на то, что свинцовые батареи могут быть вторично переработаныВторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах, является токсичным тяжёлым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны для возможности его вторичного использования.
Свинец из изношенных аккумуляторов используется для кустарной переплавки, например, при изготовлении грузил рыболовных снастей, охотничьей дроби или гирь. Для безопасности из аккумулятора следует слить электролит, для нейтрализации его остатков банки заливаются раствором пищевой соды, после чего корпус батареи разрушают и извлекают свинцовые электроды, клеммы и перемычки банок. У электродов в переплавку годится только их каркас в виде решётки, прессованная в них рассыпчатая масса — смесь соединений Pb, а не металл. Перемычки и клеммы аккумулятора могут быть переплавлены целиком.[источник не указан 629 дней] Кустарное извлечение свинца из аккумуляторов серьезно вредит как окружающей среде, так и здоровью плавильщиков, поскольку свинец и его соединения с парами и дымом разносятся по всей округе[20][21].
См. также
Примечания
- ↑ Bertrand Gille Histoire des techniques. — Gallimard, coll. «La Pléiade», 1978, ISBN 978-2070108817.
- ↑ 1 2 3 4 5 6 7 8 Свинцовые аккумуляторы. Эксплуатация: Правда и вымыслы.
- ↑ Н. Ламтев. Самодельные аккумуляторы. Москва: Государственное издательство по вопросам радио, 1936 год.
- ↑ Как отрыть автомобильный аккумулятор: делаем батарею обслуживаемой (рус.), AkkumulyatorAvto.ru (2 августа 2017). Проверено 12 августа 2018.
- ↑ Удельная электропроводность х водных растворов серной кислоты и температурный коэффициент аt. chemport.ru. Проверено 1 июля 2018.
- ↑ Концентрация и плотность серной кислоты. Зависимость плотности серной кислоты от концентрации в аккумуляторе автомобиля (рус.), FB.ru. Проверено 1 июля 2018.
- ↑ http://auto.lenta.ru/news/2006/12/19/battery/ Американцы облегчили и уменьшили аккумуляторы
- ↑ Аккумуляторы для бесперебойного питания. Статьи компании «ООО Новая система». aegmsk.ru. Проверено 12 августа 2018.
- ↑ Свинцовый кислотный аккумулятор. Устройство и принцип действия аккумулятора. (рус.). www.eti.su. Проверено 1 июля 2018.
- ↑ Расчет идеального свинцового аккумулятора.
- ↑ Свинцовый кислотный аккумулятор. Устройство и принцип действия аккумулятора. (рус.). www.eti.su. Проверено 1 июля 2018.
- ↑ ГОСТ 26881-86 Методика проверки свинцовых аккумуляторов
- ↑ Краткий аналитический обзор существующих способов оценки ёмкости ХИТ и приборов, реализующих эти способы
- ↑ ГОСТ Р 53165-2008: Батареи аккумуляторные свинцовые стартерные для автотракторной техники. Общие технические условия
- ↑ Руководство, 1983, с. 70.
- ↑ Железнодорожный транспорт. — 2011. № 12. — c.35.
- ↑ Руководство, 1983, с. 21-23.
- ↑ Вредные добавки к электролиту свинцовых аккумуляторов
- ↑ О противоречиях в теории работы свинцового кислотного аккумулятора к. т. н., проф. Кочуров А. А. Рязанский военный автомобильный институт Архивировано 20 сентября 2011 года.
- ↑ Отравление свинцом | ProfMedik Медицинский Портал (рус.). profmedik.ru (22 февраля 2016). Проверено 4 февраля 2017.
- ↑ Кочуров. http://echemistry.ru/assets/files/books/hit/statya-o-protivorechiyah-v-teorii-raboty-svincovogo-kislotnogo-akkumulyatora.pdf (рус.). Новости. Первоуральск.Ru (17 июля 2014). Проверено 4 февраля 2017.
Ссылки
Литература
- Каштанов В. П., Титов В. В., Усков А. Ф. и др. Свинцовые стартерные аккумуляторные батареи. Руководство.. — М.: Воениздат, 1983. — 148 с.
wikipedia.green
Свинцово-кислотный аккумулятор — это… Что такое Свинцово-кислотный аккумулятор?
Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: аккумуляторные батареи в автомобильном транспорте, аварийные источники электроэнергии.
История
Свинцовый аккумулятор разработал в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля. В 1878 году Камилл Фор усовершенствовал его конструкцию, покрыв пластины аккумулятора свинцовым суриком.
Принцип действия
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде.
Энергия возникает в результате взаимодействия оксида свинца и серной кислоты до сульфата (классическая версия). Проведенные в СССР исследования показали, что внутри свинцового аккумулятора протекает как минимум ~60 реакций, порядка 20 из которых протекают без участия кислоты электролита (нехимические)[1]
Во время разряда происходит восстановление диоксида свинца на катоде[2][1] и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Химическая реакция (слева направо — разряд, справа налево — заряд):
В итоге получается, что при разряде аккумулятора расходуется серная кислота из электролита (и плотность электролита падает, а при заряде, серная кислота выделяется в раствор электролита из сульфатов, плотность электролита растёт). В конце заряда, при некоторых критических значениях концентрации сульфата свинца у электродов, начинает преобладать процесс электролиза воды. При этом на катоде выделяется водород, на аноде — кислород. При заряде не стоит допускать электролиза воды, в противном случае необходимо её долить для восполнения потерянного в ходе электролиза количества.
Устройство

Элемент свинцово-кислотного аккумулятора состоит из электродов (положительных и отрицательных) и разделительных изоляторов (сепараторов), которые погружены в электролит. Электроды представляют собой свинцовые решётки. У положительных активным веществом является перекись свинца (PbO2), у отрицательных активным веществом является губчатый свинец.
На самом деле электроды выполнены не из чистого свинца, а из сплава с добавлением сурьмы в количестве 1-2 % для повышения прочности и примесей. Иногда в качестве легирующего компонента используются соли кальция, в обеих пластинах, или только в положительных. Применение солей кальция вносит не только положительные но и много отрицательных моментов в эксплуатацию свинцового аккумулятора, например, у такого аккумулятора при глубоких разрядах существенно и необратимо снижается емкость.
Электроды погружены в электролит, состоящий из разбавленной дистиллированной водой серной кислоты (H2SO4). Наибольшая проводимость этого раствора наблюдается при комнатной температуре (что означает наименьшее внутреннее сопротивление и наименьшие внутренние потери) и при его плотности 1,23 г/см³
Однако на практике, часто в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29 −1,31 г/см³.
Существуют экспериментальные разработки аккумуляторов где свинцовые решетки заменяют вспененным карбоном, покрытым тонкой свинцовой пленкой. Используя меньшее количество свинца и распределив его по большой площади, батарею удалось сделать не только компактной и легкой, но и значительно более эффективной — помимо большего КПД, она заряжается значительно быстрее традиционных аккумуляторов.[3]
В батареях для бытовых ИБП жидкий электролит сгущают водным щелочным раствором силикатов натрия (Na2Si2O4)жидкое стекло до пастообразного состояния.
Физические характеристики
Аккумулятор электромобиля- Теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 30-60.
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250.[4]
- ЭДС заряжённого аккумулятора = 2,11 — 2,17 В, рабочее напряжение = 2 В (3 или 6 секций в итоге дают стандартные 6 В или 12 В (12 В)).[1]
- Напряжение полностью разряженного аккумулятора = 1,75 — 1,8 В (из расчета на 1 секцию). Ниже разряжать их нельзя.[1]
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80-90 %
Эксплуатационные характеристики
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде[5] малым током (1/20 номинальной емкости, выраженной в А*ч).
- Стартерный ток (для автомобильных аккумуляторов). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики[6] замера отличаются, главным образом, допускаемым конечным напряжением.
- Резервная емкость (для автомобильных аккумуляторов). Характеризует время, в течение которого аккумулятор может отдавать ток 25А до конечного напряжения 10,5В согласно ГОСТ Р 53165-2008[7].
Эксплуатация
Ареометр может быть использован для проверки удельного веса электролита каждой секцииПри эксплуатации «обслуживаемых» аккумуляторов (с открываемыми крышками над банками) на автомобиле при движении по неровностям неизбежно происходит просачивание проводящего электролита на корпус аккумулятора. Во избежание сильного саморазряда необходимо периодически нейтрализовывать электролит протиранием корпуса, например слабым раствором пищевой соды или разведенным в воде до состояния консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита, что увеличивает его плотность, увеличивая напряжение на аккумуляторе, и может оголить свинцовые пластины. Поэтому необходимо следить за уровнем электролита и своевременно доливать дистиллированную воду.
Такие нехитрые операции вместе с проверкой автомобиля на утечку тока и периодической подзарядкой аккумулятора могут на несколько лет продлить срок эксплуатации батареи.
Свинцово-кислотный аккумулятор при низких температурах
По мере снижения окружающей температуры, параметры аккумулятора ухудшаются, однако в отличие от прочих типов аккумуляторов, свинцово-кислотные снижают их относительно медленно, что не в последнюю очередь обусловило их широкое применение на транспорте. Считается что свинцово-кислотный аккумулятор теряет ~1% ёмкости на каждый градус от +20°C. Т.е. в -30°C свинцово-кислотный аккумулятор будет иметь 50% ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, ростом вязкости электролита, который уже не может в полном объёме поступать к электродам, и вступает в реакцию лишь в непосредственной близости от них, быстро истощаясь.
Не полностью заряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1.10)
Хранение
Свинцово-кислотные аккумуляторы необходимо хранить только в заряжённом состоянии. При температуре ниже −20 °C заряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/секцию 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/секцию в течение 6-12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи и накипи на поверхности аккумулятора создаёт проводник для тока от одного контакта к другому и приводит к саморазряду аккумулятора,после чего начинается преждевременная сульфатизация пластин и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
Износ свинцово-кислотных аккумуляторов
При использовании технической серной кислоты и не дистиллированной воды, ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи.[8]
В результате каждой реакции образуется нерастворимое вещество — сернокислый свинец PbSO4, осаждающийся на пластинах, который образует диэлектрический слой между токоотводами и активной массой. Это один из факторов, влияющий на срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[1], заключающаяся в образовании крупных кристаллитов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с токоотводами, что приводит к опаданию активной массы;[9][1]
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности.[1]
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, самому починить нельзя, некоторые источники описывают химические растворы и прочие способы способные «десульфатировать» пластины. Простой но вредный для жизни аккумулятора способ предполагает использование раствора сульфата магния.[1] Раствор заливается в секции после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно батареи, что может привести к замыканию секции поэтому обработанные секции желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства. Если батарея имеет одну или несколько секций которые не работают (то есть не дают 2.17 вольта — например если корпус имеет трещины) возможно соединить две (или больше) батареи последовательно: к плюсовому контакту первой батареи подключаем плюсовой провод потребителя, к минусовому контакту второй батареи — минусовой провод потребителя, а две оставшихся контакта батареи соединяются кабелем. Такая батарея имеет суммарное напряжение работающих секций и поэтому количество работающих секций должно быть не более шести — то есть необходимо слить электролит из излишних секций. Такой вариант подходит для транспортных средств с большим моторным отсеком.
Вторичная переработка
Кодовый символ указывающий, что свинцовые батареи могут быть вторично переработаныВторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах является тяжелым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны на специальных предприятиях для возможности его вторичного использования.
Выброшенные аккумуляторы часто используются как источник свинца для кустарной переплавки, например, в рыболовные грузила, дробь или гири. Для этого из аккумулятора сливается электролит, остатки нейтрализуются промыванием каким-либо безвредным основанием (например, гидрокарбонатом натрия), после чего корпус батареи разбивается и извлекается металлический свинец.
См. также
Примечания
Ссылки
dic.academic.ru